Как уже говорилось в присутствии электроноакцепторных соединений, например $AlCl_3$, образуется комплекс несколько отличается от предыдущего. Если в данном случае заменить $HCl$ на $DCl$. то атом водорода кольца легко обменивается на дейтерий. Такой обмен свидетельствует об образовании $\sigma$-комплекса, в котором $H^+$ или $D$ образует истинный связь с атомом углерода кольца. Положительный заряд делокализуеться по другим пяти атомах углерода кольца с участием $\pi$-орбиталей, а атомы дейтерия и водорода расположены в плоскости, перпендикулярной плоскости кольца. Образуется структура аналогична циклопентадиенилкатиону, энергия сопряжения в котором только на $10$ ккал / моль меньше, чем у бензола и равна $26$ ккал / моль.
Доказательство существования $\sigma$-комплексов
Тот факт, что в данном случае имеет место образование двух различных комплексов, подтверждается различием в их свойствах. Образование $\pi$-комплекса не приводит к существенному изменению цвета и сопровождается незначительным изменением спектра, что свидетельствует о незначительных изменениях в электронной структуре. В присутствии $AlCl_3$ наблюдается изменение цвета к зеленому, раствор становится электропроводным, спектр поглощения толуола резко меняется.
Правильность предположения об образовании $\sigma$-комплекса подтвердили опыты, в которых удалось выделить такие $\sigma$-комплексы. В настоящее время считается общепринятым, что реакции электрофильного замещения в ароматическом ряду протекают как двухстадийный процесс по созданию $\pi$- и $\sigma$-комплексов. Образование $\pi$- и $\sigma$-комплекса аналогичное реакциям присоединения у олефинов, разница заключается только в заключительной стадии. Для ароматических соединений характерна реакция замещения, для олефинов присоединения.
Доказательством двохстадийности служит то, что при замене в субстрате водорода на дейтерий и тритий изотопный эффект практически не наблюдается. То есть присоединение электрофильного частицы и отщепление протона проходит не одновременно, при этом лимитирующей стадией является образование карбокатюна по двухстадийному механизму, где не затрагивается связь $Ar-H.$
Изомерные конфигурации переходных комплексов
В реакция с монозамещенными бензолами могут образовываться четыре конфигурации $\sigma$-комплексов - орто-, мета-, пара- и ипсо- ("ипсо" положение обозначает атаку или замещение в положение по месту уже существующего заместителя, и несущее заместители, отличные от водорода):
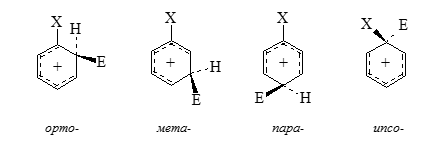
Рисунок 1.
В соответствии с этим существует четыре разных конфигурации переходных состояний, энергии которых зависят от степени взаимодействия заместителей $X$ с положительными зарядами кольца.
Ипсо-замещение
Из орто, мета и пара конфигураций комплексов может образовываться продукт замещения водорода (путем отщепления протона). Из ипсо комплекса же образовываются продукты замещения групп $X$ путем отщепления катионов $X^+$. Замещение по ипсо- положению характерно для ряда металлоорганических соединений. Это связанно стем, что металл в них замещаются легче протона:
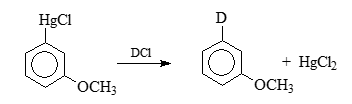
Рисунок 2.
При определенных условиях ипсо-замещение можно провести для $X=Alk$, $Br$ или $Cl$ заместителей. С другими замещенными бензолами ипсо-замещение провести не возможно, так как в этих производных заместитель должен отрываться в виде малоустойчивого катиона $X^+$. И чем выше электрофильная активность катионов $X^+$, тем хуже группы $X$ отщепляются при мономолекулярных распадах аренониевых ионов. В следующем разделе будет рассмотрено замещение протона в орто-, мета- и пара- положения в замещенных бензолах по отношению к заместителям.











