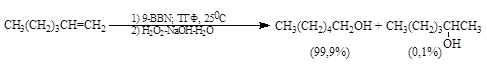
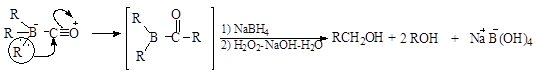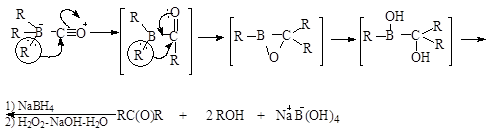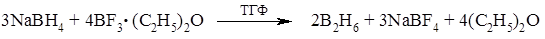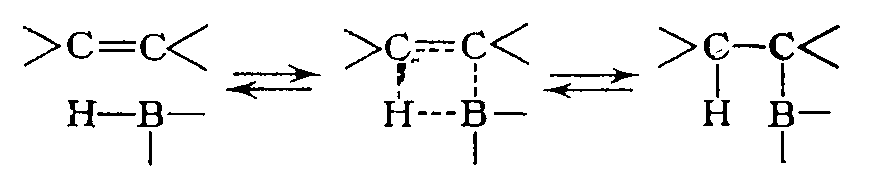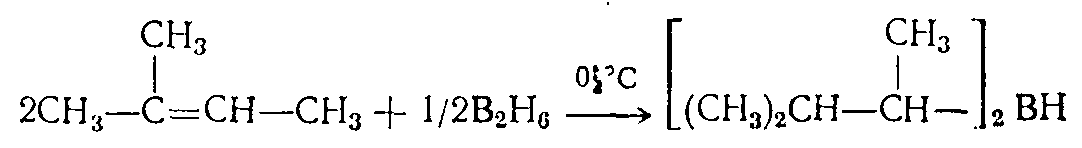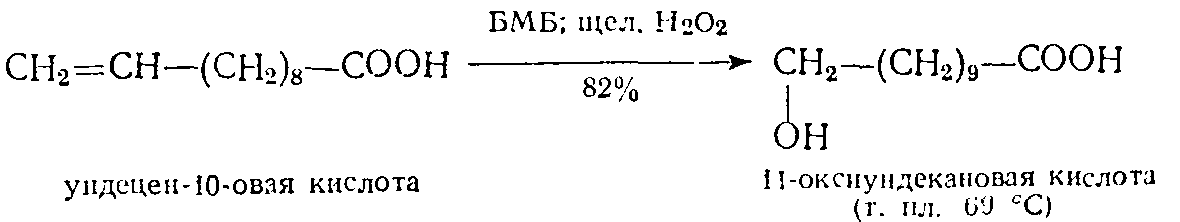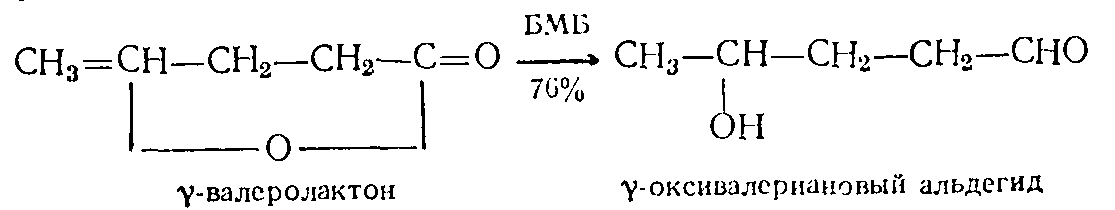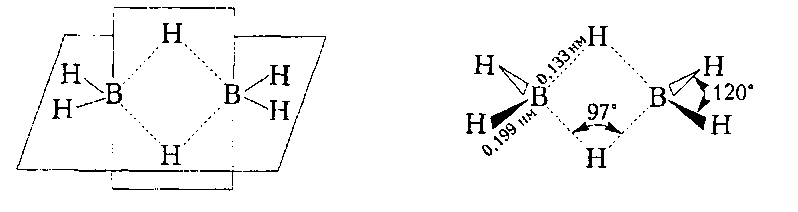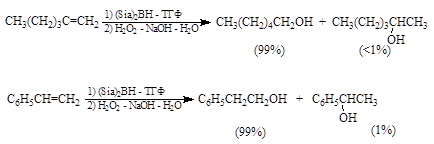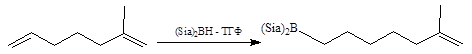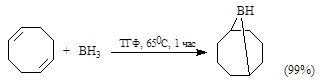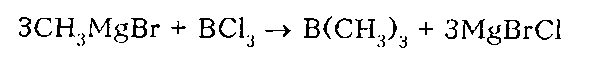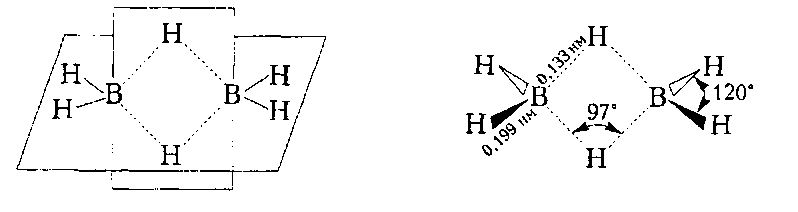Браун и Субба Рао (1959) разработали косвенный метод гидратации олефинов по месту двойной связи, первой стадией которого является гидроборирование. При обработке олефина раствором боргидрида натрия и хлористого алюминия в диметиловом эфире диэтиленгликоля образуется триалкилборан.
Первичные спирты получаются в результате восстановления под действием $NaBH_4$ интермедиатов, образующихся после миграции только одной алкильной группы:
В присутствии эквимольного количества воды реакция останавливается на стадии миграции двух алкильных групп. Последующее расщепление борэпоксида перекисным щелочным раствором приводит к симметричным кетонам:
Гидроборирование с дибораном
Другим методом гидроборирования являеться взаимодействие алкена с боранами. Например, с дибораном $B_2H_6$, который можно получить взаимодействием боргидрида натрия и трехфтористого бора.
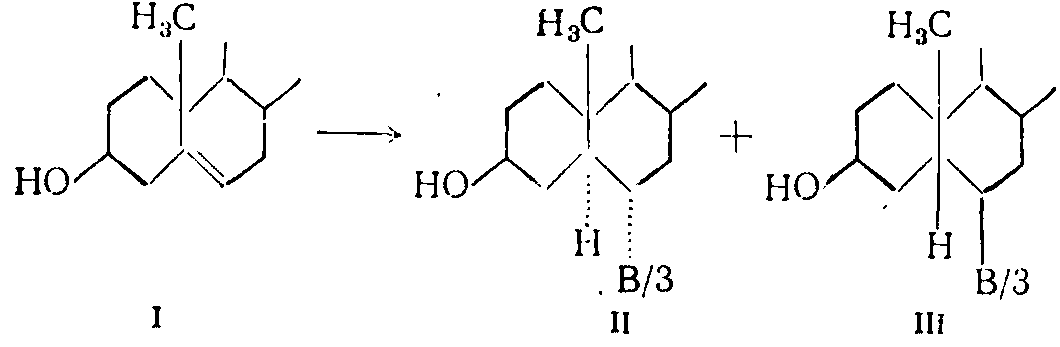
Характер присоединения в реакции гидроборирования с боранами был впервые описан Вехтером (1959). Папно применил реакцию гидроборирования к холестерину (I), использовав образовавшуюся смесь продуктов для получения производных 6-кетохолестана. В данном случае гидроборирование протекает путем цис-присоединения, при котором получаются два цис- продукта (II и III), образование которых происходит против правила Марковникова (Панно, 1959):
Отклонение от обычного правила транс-присоединения в ионных реакциях свидетельствует о том, что присоединение протекает через циклическое переходное состояние:
С помощью бис-3-метил-2-бутил бора на (БМБ), который образуется даже в присутствии избытка олефина по реакции
можно увеличить выходы менее затрудненных продуктов и проводить реакции селективного восстановления, которые нельзя осуществить другим способом (Браун, 1961). Поскольку этот реагент не восстанавливает карбоксильную группу, его можно использовать для непосредственного гидроборирования кислот:
$\gamma$-Лактоны реагируют только с одним молем реагента, даже если последний присутствует в избытке:
$(Sia)_2BH$ позволяет селективно гидроборировать концевую двойную связь в присутствии других двойных связей:
В препаративных целях вместо $(Sia)_2BH$ удобнее использовать бициклическое соединение 9-бора-бицикло[3.3.1]нонан (9-ББН) получаемое по схеме:
9-ББН негорючее вещество, но оно окисляется на воздухе. Твердый 99-бора-бицикло[3.3.1]нонан гораздо термически стабильнее алифатических боранов.
Борорганические соединения
Борорганические соединения (БОС) за последние 30 лет переживают бурное развитие благодаря своим уникальным свойствам и синтетическим возможностям.
БОС рассматривают как производные бороводородов вроде борана $BH_3$, диборана $B_2H_6$ и др. Боран, например, может создать три вида производных $RBX_2$, $R_2BX$, $R_3B$, где X = галогены, $-OН$, $-OR'$, $-NR'_2$ и тому подобные.
Борорганические соединения синтезируют в основном в соответствии с методами получения элементоорганических соединений алкилированием или арилированием галогенидов бора, эфиров борной кислотоы с элементоорганическими соединениями:
Соединения бора проявляют сильные электронно-дефицитные свойства, что связано с особенностями их строения. Так, боран $BH_3$, в свободном состоянии не существует, а находится в виде димера $B_2H_6$:
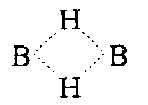
Это обусловлено тем, что атом бора имеет на внешней электронной оболочке всего три электрона и в молекуле $BH_3$ для устойчивости октета ему не хватает двух электронов. Поэтому связи в молекуле диборана образуются иначе, чем классические ковалентные связи. Как установил В. Лилскомб (1959), в молекуле диборана два атома бора и четыре атома водорода расположены в одной плоскости и соединены между собой обычными двухцентровыми двухэлектронными локализованными ковалентными связями. Два других атома водорода с одним электроном каждый расположены в плоскости, перпендикулярной к предыдущей, в вершинах ромба. Эти атомы водорода и два атома бора с одним остаточном электроном для каждого образуют две трехцентровые двухэлектронные связи (две молекулярные орбитали), или два мостовых связи В ••• Н ••• В, такие связи в методе МО называются четырехэлектронными:
Приведенные особенности строения связей молекулы диборана упрощены, поскольку трехцентровые двухэлектронные орбитали являются только частью многоцентровой делокализованной молекулярной орбитали диборана. При полном описании формирования МО используются АО двух атомов бора и шести атомов водорода. Два атома водорода, образующие мостиковые связи, менее реакционноспособны и, как установлено методами рентгенографии, электронографии, КР- и ИК-спектроскопии, отличаются от четырех других атомов водорода значениями длины связей и валентных углов. Поэтому, если эти четыре атома водорода будут замещены алкилом, структура трансформируется в производные боранов $B(R)_3$, для которых мостовые структуры не характерны.
Борорганические соединения, в отличие от элементоорганических соединений щелочных металлов, инертнее, и не расщепляются под действием воды, растворов кислот и щелочей, но легко расщепляются при действии низких карбоновых кислот. Вследствие своей електроноакцепторний природы борорганические соединения легко взаимодействуют с нуклеофилами с образованием комплексов с семиполярной связью.
Соединения бора используют не только для органического синтеза, но и как эффективное ракетное топливо.