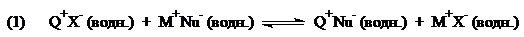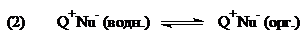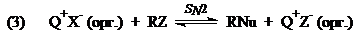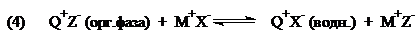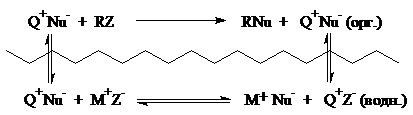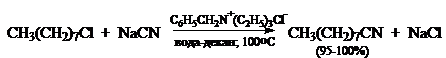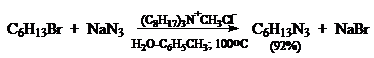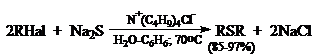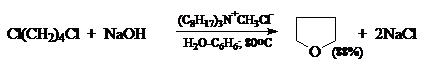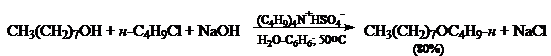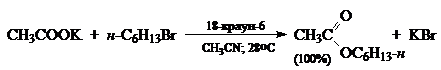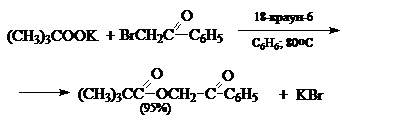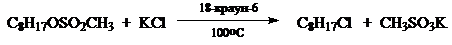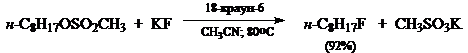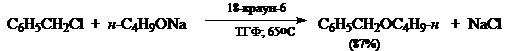Межфазный катализ (МФК) является простым и доступным способом активации нуклеофилов, в нем нуклеофильные реагенты переносятся из водных растворов в малополярные органические среды ($CHCl_3$; $CH_2Cl_2$; $C_6H_5CH_3$; $C_6H_6$ и др.), которые не смешиваются с водой. Межфазный катализ был внедрен органическую химию благодаря работам М. Макоши, Ч. Старкса и А. Брендстрема. Основную идею межфазного катализа можно наблюдать на примере простейшей реакции бимолекулярного нуклеофильного замещения в субстратах $RZ$ при взаимодействиях с нуклеофильными реагентами $Nu^-.$
Используют две несмешивающиеся фазы — водную и органическую. В водяною фазу вводят соли $M^+Nu^-$. В органическую фазу вводят субстрат $RZ$, который будет реагировать с нуклеофилами $Nu^-.$
Закономерности протекания межфазного катализа
Соли $M^+Nu^-$, где $M$= щелочные металлы, совершенно нерастворимы в неполярных органических растворителях, составляющих органическую фазу, поэтому в отсутствии процесса межфазного катализа никаких взаимодействий между $RZ$ и $Nu^-$ не происходит. В эту смесь вводятся катализаторы межфазного переноса — хлориды или бромид ы тетраалкил- аммония $R_4N^+Cl^-$, $R_4N^+Br^-$ или тетраалкил- фосфония $R_4P^+Cl^-$. В этих соединениях катионы солей являются липофильными, а анионы — гидрофильными. Липофильные катионы обладают способностью находиться как в водной, так одновременно и в органической фазах. Первоначально в водной фазе происходит процесс анионного обмена между солью тетраалкиламмония и исходными нуклеофильными реагентами $M^+Nu^-$:
где $Q^+ = R_4N^+$ или $R_4P^+.$ Затем происходит переносы солей $Q^+Nu^-$, содержащих требуемые нуклеофилы $Nu-$, из водной в органическую фазу. Липофильные свойства катионов $Q^+ (R_4N^+$; $R_4P^+)$ способствуют процессам межфазных переносов солей:
Далее в органической фазе и происходит реакция нуклеофильного замещения:
И затем цикл завершается регенерацией солей $Q^+X^-$ и переносом их в водную фазу:
Классическая схема каталитического цикла с межфазным переносом
Классическую схему каталитического цикла с межфазным переносом можно представит, согласно Ч. Старксу, следующим образом:
где $Q^+$ — катионы тетраалкиламмония или фосфония, $Nu^-=$ соответствующие анионы ($CN^-$; $NO_2^-$; $N_3^-$; и т.д.). В этом цикле соли $Q^+Z^-$, которые генерируются в органической фазе, не обязательно должна быть идентичны солям, первоначально вводимым в качестве катализатора. Обязательными условиями являются наличие липофильных катионов $Q^+$ и обмен анионона $Z^-$ и $Х^-$ на анионы нуклеофилов $Nu^-.$
Межфазные катализаторы
В качестве межфазных катализаторов могут выступать только такие соли, в которых катионы могут находиться как в водной, так и в органической фазе. Этому удовлетворяют четвертичный ион $R_4N^+$, а также ион $R_4P^+$ где $R$ - алкильные группы, содержащие от 4 до 10—16 атомов углерода, с симметричным, так и несимметричным строением. Среди них наибольшее распространение получили $C_6H_5CH_2N^+ (C_2H_5)^3Cl^-$; $(C_8H_{17})_4N^+ Br^-$; $(C_4H^9)_4N^+ C_1^-$; $C_{16}H_{33}N^+ (CH_3)_3Вr^-$ и другие аммониевые и фосфониевые соли.
В малополярных органических растворителях должны образовыватся контактные ионные пары $R_4N^+Nu^-$, обладающие очень высокими реакционными способностями. Высокой нуклеофильности анионов $Nu^-$ в малополярных органических растворителях способствует то, что они практически не сольватированы в этих средах и они обладают большими межионными расстояниями (до 5 Å), т.е. недостаточно сильными электростатическими стабилизациями анионов в ионных парах.
Простейшим примером реакций $SN_2$-замещения с межфазным катализом является синтез нитрилов при взаимодействиях алкилхлоридов и бромидов с $NaCN$ в бинарных системах вода - жидкие алканы (например, декан). В качестве катализатора используют бензилтриэтиламмоний-хлорид (ТЭБАХ — катализатор Макоши).
Метод межфазного катализа эффективен и для многих других реакций протекающих по $SN_2$ механизму, например:
Межфазный катализ с краун-эфирами и их производными
МФК не ограничен переносом реагентов только в жидких фазах. Перенос реагентов из так называемой «твердой фазы» в жидкую фазу также возможен в ряде процессов межфазного катализа.
В данном случае подразумевается использование катализатора межфазного переноса с особенной природой. В качестве такого катализатора можгут выступать новые комплексообразующие агенты - макроциклические полиэфирные вещества, называемые краун-эфирами (от англ. crown - корона), а также их аналоги. Наиболее часто используют, уже рассмотренный ранее 18-краун-6, а также 15-краун-5 и [2,2,2]-криптанд (первая цифра в названиях краун-эфиров означает размеры циклов, вторая - количество атомов кислорода):
Общей чертой для всех краун-эфиров, и им родственных соединений будет геометрическаю структура их молекул, которая включает в себя полость внутри цикла (или соединений циклов.
Каталитический перенос нуклеофильного реагента из твердой фазы в жидкую особенно важен в случаях когда в качестве нуклеофила выступают группы $F^-$, $Cl^-$, $RCOO^-$ - являющиеся жесткими нуклеафилами, а также групп промежуточной жесткости, таких как $N_3^-$. Применение краун-эфира в такой реакции позволяет проводить синтез с высоким выходом.
Ниже приведены примеры реакций, протекающих по таким условиям:
МФК нашел применение в самых разнообразных областях органического синтеза. Его применяют в процессах присоединения дихлоркарбенов к двойным связям алкенов, окисления алкенов и алкилбензолов и т.д.