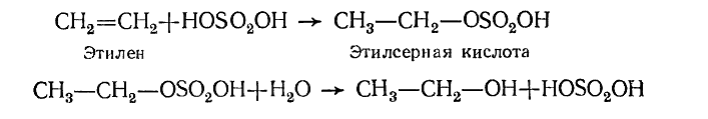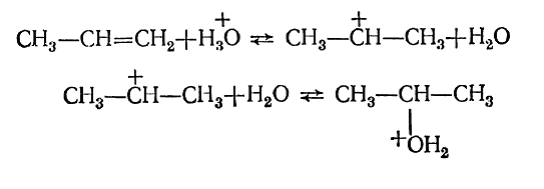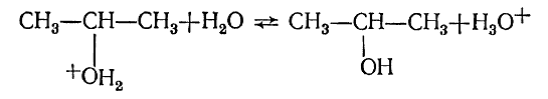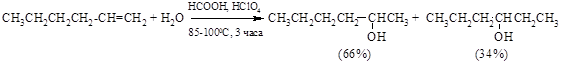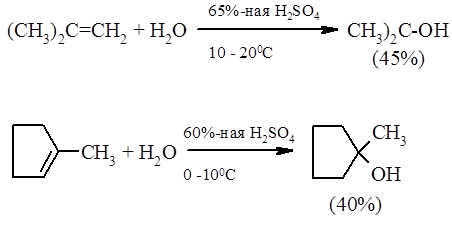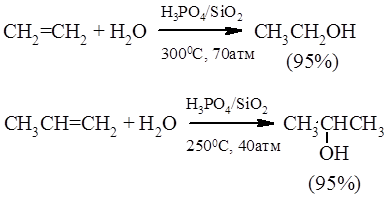Концентрированная серная кислота при комнатной температуре присоединяется по двойной $C=C$ связи алкенов с образованием алкилсерных кислот, легко гидролизующихся на спирт и серную кислоту:
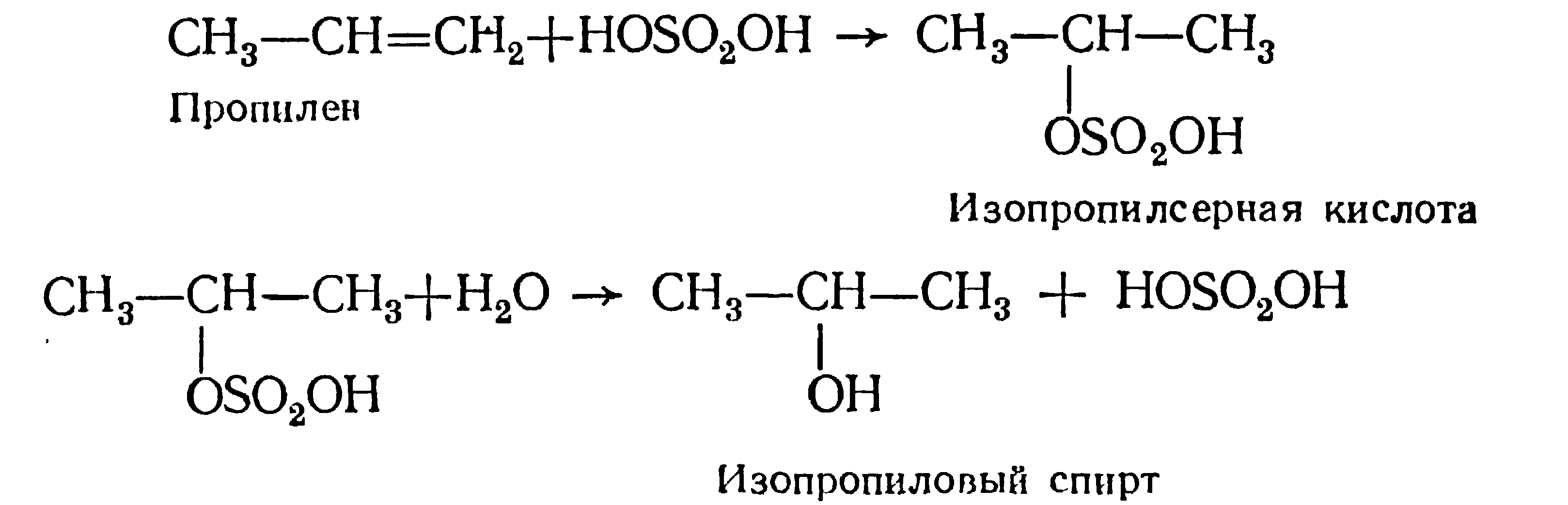
К несимметричным гомологам этилена серная кислота присоединяется в соответствии с правилом Марковиикова:
Механизм каталитической гидратации
Механизм каталитической гидратации включает присоединение на первой стадии иона гидроксония с образованием карбокатиона. Источником аниона является вода. При этом образуется протонированный спирт, который на следующей стадии отдает ион водорода другой молекуле воды:
Восстановление двойной связи $C=C$ проводят чаще всего в присутствии таких гетерогенных катализаторов, как благородные металлы: палладий, нанесенный на тонкоизмельченный древесный уголь, родий, никель, рутений, оксид платины $PtO_2$ (катализатор Адамса).
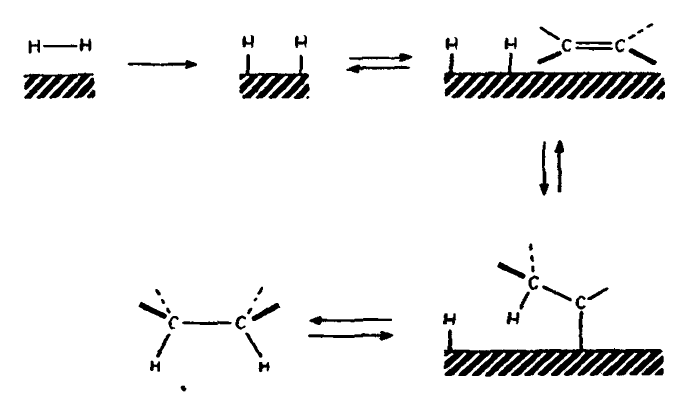
Механизм этого процесса включает в себя химическую сорбцию молекулы водорода с последующим ее гомолитическим разрывом (диссоциацией). Олефин взаимодействует с поверхностью катализатора своей наименее пространственнозатрудненной стороной. Реакция присоединения протекает в две стадии (что было показано при помощи изотопного обмена ($H_2$ - $D_2$), т. е. происходит поочередное присоединение двух атомов водорода, адсорбированных на поверхности катализатора. Таким образом, возникают продукты цисгидрирования с наименее пространственнозатрудненной стороны.
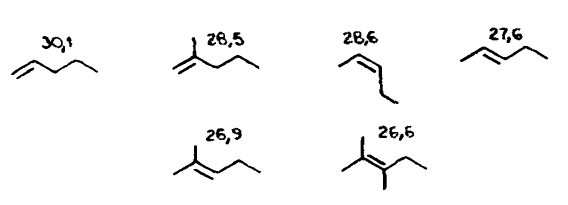
Изменение энтальпии $ΔH^0$ процесса гидрирования составляет величину порядка 30 ккал/моль. Эта цифра характеризует термодинамическую стабильность олефинов: транс > цис; тетра > три > > ди > монозамещенные.
Склонность вторичных алкильных карбокатионов к перегруппировкам мешает использованию гидратации алкенов для получения вторичных спиртов:
Этот метод в лаборатории нашел ограниченную область применения только для получения третичных спиртов:
Получение этилового и изопропилового спиртов
Гидратация простейших алкенов – этилена и пропилена – представляет собой важный промышленный метод получения этилового и изопропилового спиртов:
Метод производства этилового спирта гидратацией этилена, получаемого при крекинге нефти, почти полностью вытеснил метод брожения. Гидратация этилена заключается в поглощении олефина серной кислотой с последующим гидролизом алкилсерной кислоты и выделением спирта фракционированием. На практике работают в широких интервалах температур, концентраций кислоты и молярных соотношений компонентов, поскольку каждый завод приспосабливает технологию производства в зависимости от доступности кислоты и олефина и легкости использования отработанной кислоты. В качестве побочного продукта производства синтетического спирта получается значительное количество эфира.
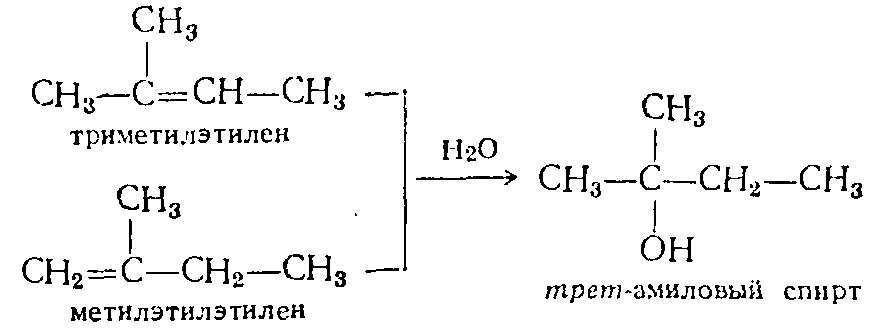
Олефины можно также гидратировать каталитически в водных растворах серной или азотной кислоты низкой концентрации, тогда промежуточного образования соответствующих эфиров не происходит. Эта реакция была подвергнута кинетическому исследованию для выяснения ее механизма. Один из предложенных механизмов заключается в том, что присоединяющийся протон должен отщепиться от иона гид роксония прежде, чем он сможет принять участие в определяющей скорость реакции стадии образования карбониевого иона. В другом возможном механизме реакции первая стадия представляет собой быстрое и обратимое образование πкомплекса, который затем медленно изомеризуется в карбониевый ион. Последний быстро реагирует с водой с образованием спирта и регенерацией иона гпдроксония. Этот механизм был подтвержден при изучении гидратации триметилэтилена и метилэтилэтилена; оба олефина превращаются в третамиловый спирт:
Если реакции остановить, когда превращение прошло на 50%, то регенерируется исходный олефин. Таким образом, не происходит взаимного превращения олефинов в результате быстрого и обратимого обра зования обычного карбониевого иона.
В лабораторной практике прямая гидратация алкенов не нашла широкого применения как вследствие жестких условий, так и благодаря образованию значительного количества изомерных спиртов. В настоящее время для региоселективного получения спиртов из алкенов обычно используется родственная реакция оксимеркурирования – демеркурирования.