Зависимость стабильности карбанионов от термодинамической кислотности
Соединения, в состав которых входят (-М)-заместители- карбонильная, нитрильная или нитрогруппа, имеют высокую $CH$-кислотность.
(-М)-заместители обладают способностью стабилизировать карбанионы путем делокализации заряда:
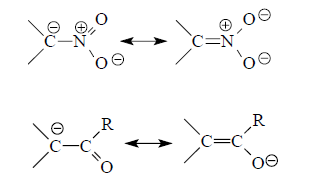
Рисунок 1.
При термодинамической кислотности величины кислотности $pka$ не зависят от механизма переноса протона.
Для эффективного сопряжения важна конфигурация карбаниона. У него должна быть возможность принять плоскую структуру.
Бициклический $\beta $-кетон бицикло[2.2.2]октан-2,6-дион является слабой $CH$-кислотой. Его конфигурация не плоская:
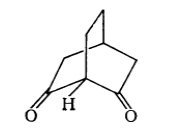
Рисунок 2.
Электронная пара жестко зафиксирована в карбанионе на $sp^3$-орбитали, поэтому перекрывание с $\pi $-орбиталями карбонильных групп произойти не может.
При ионизации моноциклического дикетона $1,3$-циклогександиона, конфигурация плоская, присутствует сопряжение и сильно выражены кислотные свойства (в воде $pka=5,26$):
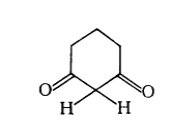
Рисунок 3.
По способности усиливать кислотность $CH$-связи (-М)-заместители располагаются в ряд:
При наличии в молекуле нескольких заместителей, обладающих ацидифицирующими свойствами, кислотность $CH$-связи еще более возрастает. Однако кислотность будет возрастать не пропорционально числу групп, так как расположить все атомы в одной плоскости невозможно.
Сильно повышают кислотность соседней $CH$-связи заместители, подобные --$CN$, -$COR$ , $NO_2$, так как в формирующемся карбанионе в результате сопряжения отрицательный заряд в основном переходит от неэлектроотрицательного углерода к электроотрицательным кислороду или азоту. Чистые углеводороды также могут обладать высокой кислотностью.
Циклопентадиен обладает высокой кислотностью ($pka$ в ДМСО=$18$), что обусловлено сильным сопряжением в карбанионе. Неподеленная электронная пара в циклопентадиенильном анионе входит в ароматическую шести-$\pi $-электронную систему и делокализуется по всем атомам кольца:
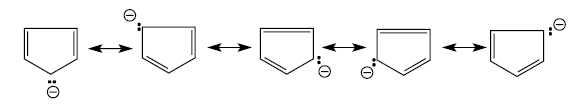
Рисунок 4.
Углеводороды Куна
Семейство сопряженных ненасыщенных углеводородов, которые в водных растворах проявляют кислотность, схожую с кислотностью фенолов и карбоновых кислот, называют углеводородами Куна. Соответствующие им карбанионы часто включают циклопентадиеновый фрагмент, дающий ароматический характер. Карбанионы проявляют свойства сильно сопряженных систем.
Например:
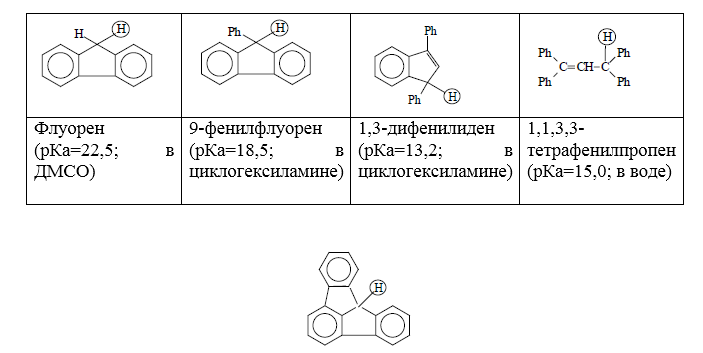
Рисунок 5. Флуораден, $pka$: в воде -- $15,0$; в $MeOH$ -- $13,5$; в ДМСО -- $13,8$
Наиболее кислые свойства проявляются у углеводородов, в которых отрицательный заряд карбаниона может быть делокализован на атомах карбона циклопентадиенового кольца.
Бензолу будет изоэлектронен анион циклогексадиена, нафталину- анион индена, фенантрену -- анион флуорена:
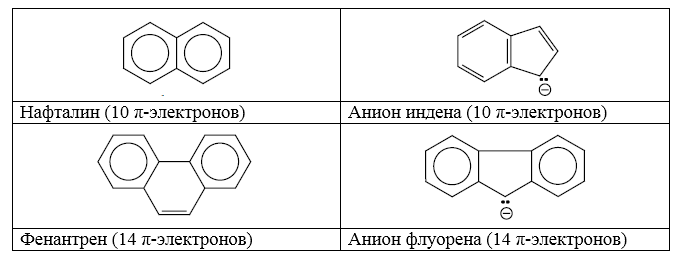
Рисунок 6.
Антиароматичность
Системы, которые дестабилизированы за счет делокализации называют антиароматическими системами.
Было установлено, что несмотря на то, что циклопропенил-анион является аллильным анионом, он менее устойчив, чем циклопропил -- анион. Делокализованный квадратный плоский циклобутадиен менее устойчив, чем его локализованная прямоугольная форма.
Антиароматическая молекула находится в состоянии, которое обладает большей энергией, чем рассчитанная или найденная энергия для модельной системы.
В основном состоянии у циклопропенил -- аниона энергия более высокая, чем энергии циклопропил- и аллил -- анионов --модельных систем.
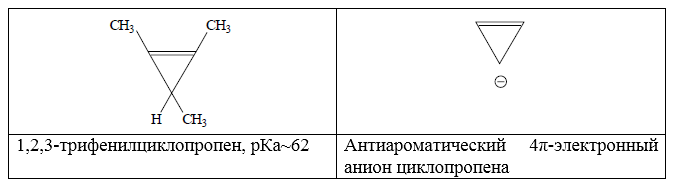
Рисунок 7.
Производные циклопропена имеют очень высокие значения $pka$.
При сопряжении могут перекрываться $p-$ и $d$-орбитали:
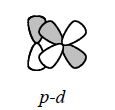
Рисунок 8.
Стабилизация за счет $p-d$-сопряжения характерна для анионов, которые содержат серу и фосфор.
Две фосфониевые группы способны стабилизировать анионный заряд так сильно, что бис-(трифенилфосфоний)метан становится двухосновной $CH$-кислотой:
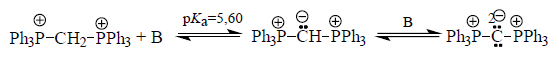
Рисунок 9.











