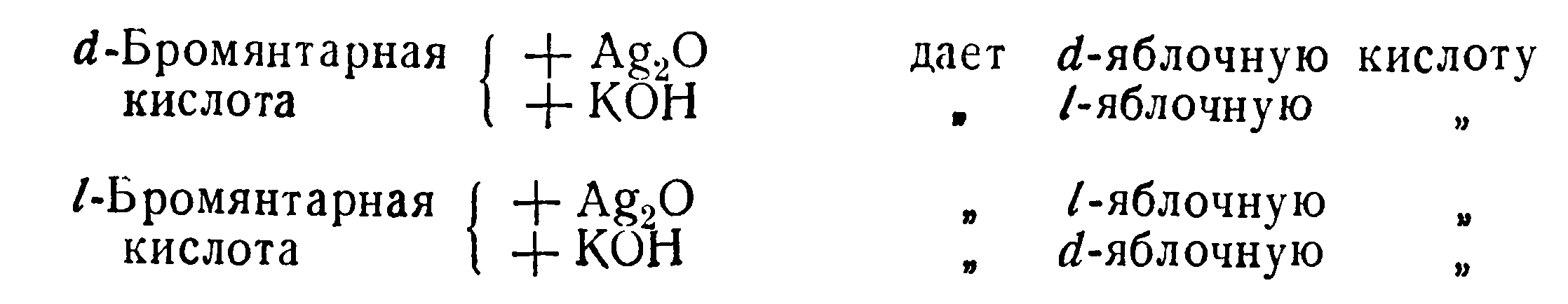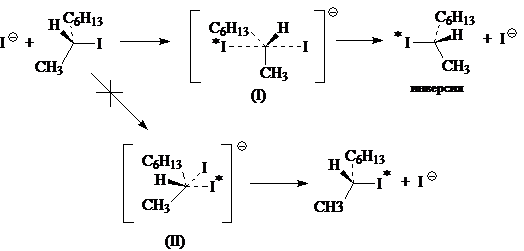Вальденовское обращение (Вальденивське инверсия, англ. Walden inversion) - инверсия конфигурации асимметричного центра молекулы при химической реакции, когда химическая форма где $X$-углерод, имея исходное тетраедральное расположение связей по $X$, превращается в химическую форму, которая имеет противоположную относительную конфигурацию. Вальденовское обращение характерно для $SN_2$ реакций, в которых при тетраэдрическом атоме углерода вхождение реагента и отщепление уходящей группы происходят синхронно и таким образом, что реагент входит со стороны, противоположной отходящей группы, следствием чего наступает обращение хиральной конфигурации.
В реакциях $SN_1$, промежуточными соединениями в которых выступают карбениевые ионы, вероятная атака с каждой из двух сторон плоскости создаваемого иона, и наблюдается полная или частичная рацемация.
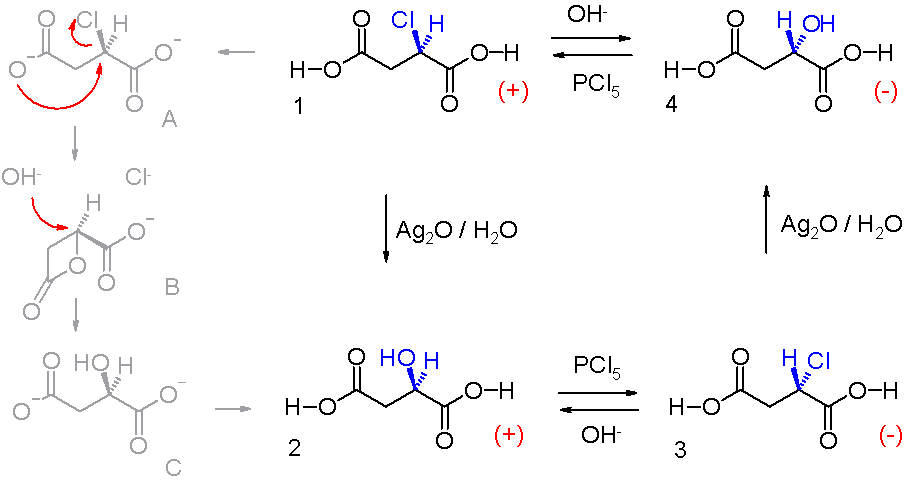
Наличие такой инверсии при химического преобразования иногда указывают в химическом уравнении с помощью стреловидного символа от реактантов к продуктам, как указанно на представленной здесь схеме. В качестве классического примера рассматривается взаимодействие (-)-гидроксиянтарной (яблочной) кислоты с $PC_{15}$ , с образованием (+)-хлорянтарной кислоты; параллельно с этим рассматривают действие тионилхлорида на (-)-гидроксиянтарную кислоту, в результате чего получается (-)-хлорянтарная кислота:
История открытия
П. Вальден в 1898—1899 гг. на основании своего наблюдения сделал вывод, что превращения активной бромянтарной кислоты в яблочную под действием щелочи происходит нормально, т. е. без изменения конфигурации, а под действием окиси серебра, напротив, аномально.
При дальнейшем исследовании этого явления были обнаружены как и другие примеры такого же взаимодействия, так и реакции не протекающие по этому правилу.
Так, окись серебра действует на $α$-бромпропионовую кислоту оптически иначе, чем на $α$-бромпропионилглицин. Ранее считалось, что это взаимодействие так происходит из-за различных расстояний между карбоксилом и галогеном. А то, что в других реакциях, протекающих иначе, объяснялост специфическими стерическими взаимоотношениям. Например в реакции $α$-бромизовалерианой кислоты и $α$-бромизовалерилглицина под действием окиси серебра они претерпевают одинаковое превращение, и здесь различное расстояние между карбоксилом и бромом не оказывает никакого влияния.
Тот же момент был использован и для случая с одинаковым поведением α-бромизовалериановой кислоты под действием щелочей и окиси серебра.
В качестве второго примера подобного рода была рассмотрена активная $β$-хлормасляная кислота, которая под действием горячей воды и под действием окиси серебра дает одну и ту же $β$-оксимасляную кислоту 5, так как вода и щелочи действуют, как правило, в одном направлении.
В этом случае такое исключение из правила также объяснялось большим расстоянием между карбоксилом и галогеном.
Об истинной причине вальденовского обращения данные предположения, конечно, ничего не говорили, поскольку мы вообще об этом ничего определенного не знаем.
В дальнейшем в отношении некоторых случаев, например для превращения дибромянтарной кислоты в винную, этот вопрос решился эксперементальным путем.
А. Вернер, который, на основании фактов, касающихся стерического протекания процесса замещения, выдвинул особую гипотезу. Поскольку он различал определенные направления действия центрального атома углерода, а именно по четырем плоскостям тетраэдра, он пришел к выводу, что вальде- новское обращение происходит лишь в том случае, когда притяжение со стороны атома углерода осуществляется в той плоскости, которая лежит напротив замещаемой группы.
Подобное представление не давало большого выигрыша, поскольку его не удавалось привести в соответствие с установленными фактами. Все же достоинством гипотезы является ее наглядность. Она имела, однако, и серьезный недостаток, который состоит в определенной ограниченности, она не охватывала всего явления в целом.
Кроме притяжения со стороны центрального атома углерода определенное влияние, по представлениям того времени, оказывали следующие моменты:
- Притяжение со стороны присутствующих замещающих групп, направленное на присоединяемую группу; таким примером может служить отчетливое влияние замещающих групп на структуру и конфигурацию полимолекул.
- Заполнение пространства существующими замещающими группами, которое, играет здесь такую же роль, как при так называемых «стерических помехах».
Из этих представлений видно, с каких различных точек зрения можно рассматривать вальденовское обращение.
Развитие теории вальденовского обращения
Прямое подтверждение того что механизм $SN_2$ происходит через вальденовское обращение было получено Хьюзом и Ингольдом. Ими была измерены скорости изотопных обменов галогенов и скорости рацемизации оптически активных 2-йодоктана, 1-фенилэтилбромида и 2-бромпропионовой кислоты при действии радиоактивных $NaI$ или $LiBr$ в ацетоне:
Скорости обмена определялись путем измерения интенсивностей радиоактивного излучения алкилгалогенидов или галогенидов щелочного металла, скорости рацемизации — с помощью поляриметра по изменению углов вращения плоскополяризованного света. Во всех случаях скорость обмена и скорость потери оптической активности были равны, следовательно, замещение происходит с инверсией конфигурации, и каждому акту нуклеофильной атаки обязательно соответствует инверсия конфигурации. Отсюда следует, что переходное состояние в $SN_2$-реакциях имеет структуру ($I$).
Современное представление об вальденовском обращения
В настоящее время установлено, что замещение через переходное состояние типа ($I$), т.е. с атакой нуклеофила с тыльной стороны по отношению к уходящей группе, является общим правилом для всех $SN_2$-реакций независимо от их зарядного типа. Даже в тех случаях, когда в исходном субстрате на уходящей группе имеется положительный заряд, а нуклеофил заряжен отрицательно, и из электростатических соображений фронтальная атака через переходное состояние типа (II), казалось бы, должна быть более предпочтительной, реакция все равно происходит с инверсией конфигурации. Это легко проиллюстрировать следующим примером:
Таким образом, можно сформулировать следующее общее правило: бимолекулярные реакции нуклеофильного замещения происходят с инверсией конфигурации реакционного центра субстрата.