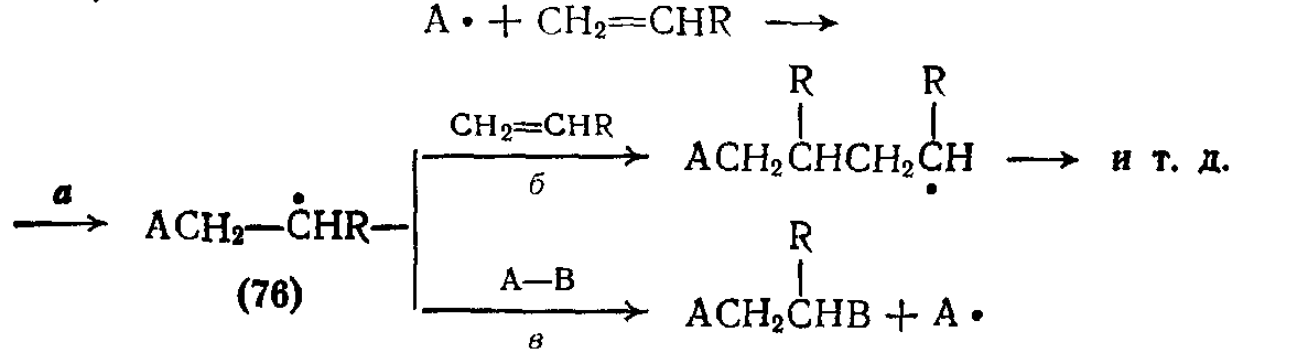
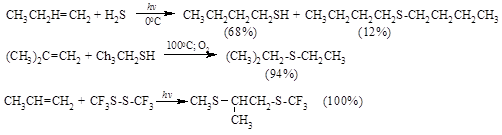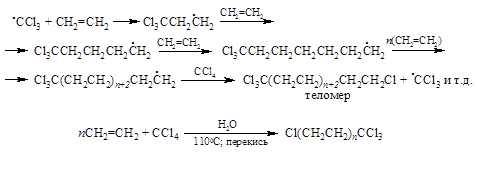Присоединение свободного радикала к олефину приводит к появлению нового радикала, который может присоединиться ко второй молекуле олефина (стадия б), затем к следующей и т. д., что ведет к теломеризации или к полимеризации. Однако радикал может взаимодействовать также и с субстратом (стадия в, стадия переноса). Повторение стадий представляет собой цепной радикальный процесс присоединения А—В к олефину
Соотношение между полимеризацией и образованием аддукта 1:1 чрезвычайно сильно зависит от природы олефина и присоединяющегося вещестаа. Объем этого раздела не позволяет подробно обсудить термодинамические факторы; ниже рассмотрены коротко и упрощенно только наиболее важные моменты. Более активные олефины, особенно те, которые образуют устойчивые радикальные аддукты, например стирол (образуется бензильный радикал) или бутадиен (образуется аллильный радикал), реагируют предпочтительно по пути б. Маршрут в благоприятен в тех случаях, когда энергия разрыва связи А—В мала, а энергия вновь образовавшейся связи с В относительно аелика, в результате чего эта стадия становится экзотермичной. Для получения продуктов 1: 1-присоединения в условиях радикального цепного процесса были успешно использованы разнообразные соединения типа А—В . Протеканию таких реакций присоединения благоприятствует проведение их в неполярных растворителях или в газовой фазе. Присоединение ускоряется светом, добавками радикальных инициаторов и нагреванием. Большинство присоединяющихся молекул относятся к типу А—Н или А—галоген, где А * — относительно устойчивый свободный радикал. Для успешного завершения стадии переноса цепи в, которая представляет собой замещение В в А—В радикалом, необходимо, чтобы В было простой частицей, такой, как водород или галоген. Другим фактором, увеличивающим соотношение между 1:1-присоединением и полимеризацией, является, естественно, наличие избытка А—В.
Ориентация присоединяющейся группы в случае несимметричных олефинов определяется тем, что радикал А- на стадии а присоединяется обычно к менее замещенному атому углерода. Классическим примером этого, так называемого антимарковниковского, присоединения является присоединение бромистого водорода к олефинам в присутствии пероксидов, которое было открыто Каратом и Майо в 1933 г.. Такую ориентацию объясняют обычно тем, что главную роль играет устойчивость образующегося радикала. Поскольку из двух возможных радикалов более замещенный является более устойчивым, то присоединение на стадии а происходит против правила Марковникова.
Стереохимия радикального присоединения
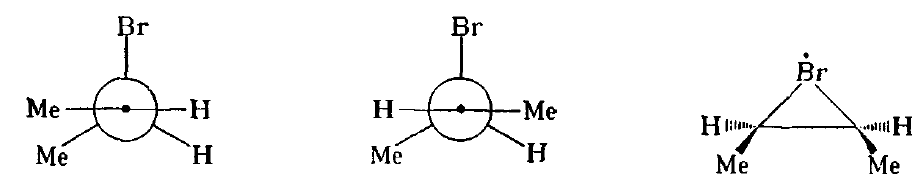
Стереохимия радикального присоединения также нуждается в некоторых пояснениях. В благоприятных условиях достаточно отчетливо проявляется тенденция к анти-присоединению А—В, в то же время в других случаях, например при катализуемом пероксидами присоединении $DBr$ к цис- и транс-бутенам-2, анти-присоединение преобладает только при -70°С, а при повышении температуры присоединение проходит нестереоспецифично. Возможно, что этот результат отражает положение конформационного равновесия между промежуточными радикалами и, которые образуются из цис- и транс-олефинов, соответственно. Роль этого равновесия увеличивается при повышении температуры. Присоединение на стадии в проходит, вероятно, со стороны, противоположной уже вошедшему в молекулу объемистому атому $Br$. Согласно другой точке зрения, анти-присоединение контролируется образованием мостикового радикала типа , обратимое превращение которого в «открытый» радикал при повышении температуры приводит к потере стереоспецифичности:
Гемолитическое присоединение к ненасыщенным системам. Присоединение галогеноводородов
Гемолитическое присоединение галогеноводородов к олефинам легко проходит только в случае бромистого водорода. Эта реакция имеет историческое значение, так как именно в этом случае было впервые установлено, что такие реакции могут протекать как по ионному, так и по радикальному механизму. Наиболее важными стадиями радикального механизма являются присоединение и стадия передачи цепи
Стадия присоединения:
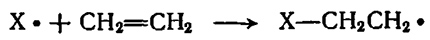
Стадия передачи цепи:
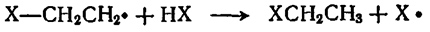
только в случае бромистого водорода как стадия присоединения, так и стадия передачи цепи являются экзотермичными. Из этого следует, что присоединение хлористого и йодистого водорода может проходить по радикально-цепному механизму только в особых случаях.
Региоспецифичность таких гомолитических процессов важна, поскольку они протекают против правила Марковникова. Поэтому, изменяя условия проведения реакции, можно получать структурные изомеры

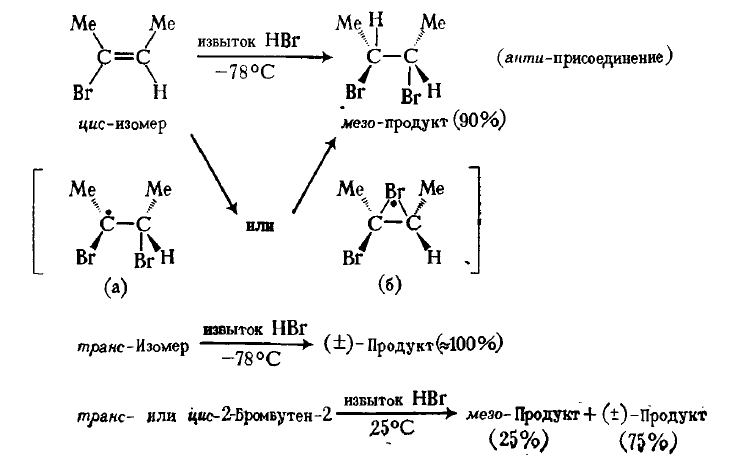
В определенных пределах можно контролировать также и стереоспецифичность реакции, так как при низких температурах и высокой концентрации бромистого водорода можно наблюдать иногда стереоспецифическое анти-присоединение. Однако при более высоких температурах и более низких концентрациях бромистого водорода стереоспецифичность процесса понижается:
Эти наблюдения могут быть истолкованы одним из двух образов: при низких температурах протекает почти синхронное анти-присоединение бромистого водорода с образованием на промежуточной стадии либо радикала (а), который только в очень малой степени подвергается инверсии или вращению, либо мостикового радикала (б). При более высоких температурах инверсия или вращение в радикале (а) протекает быстрее и соответственно вероятность образования интермедиата типа (б) уменьшается. В любом случае реакция, оставаясь стереоселективной, перестает быть стереоспецифической.
Присоединение других соединений по радикальному механизму
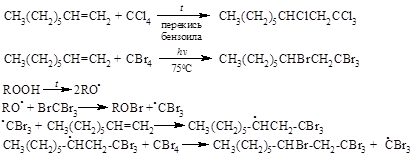
Ряд других соединений с подходящей энергией связи могут присоединяться к двойной связи по радикальному механизму, подобному радикальному присоединению HBr к алкенам. Известны многочисленные примеры присоединения к алкенам сероводорода, тиолов, дисульфидов, четыреххлористого и четырехбромистого углерода, $CBrCl_3$:
CCl4 и CBr4 легко реагируют с алкенами в присутствии перекисей, иницирующих радикальные процессы, с образованием аддуктов состава 1:1.
В некоторых случаях, особенно для самого этилена, такие реакции приводят к сложной смеси продуктов так называемой теломеризации, где промежуточно образующийся радикал присоединяет одну за другой несколько молекул этилена:
где $n = 1 (9\%); n = 2 (57\%); n = 3 (24\%)$
В процессах теломеризации преобладают продукты со сравнительно низкой молекулярной массой, соответсвующей низким значениям n