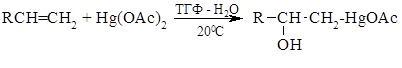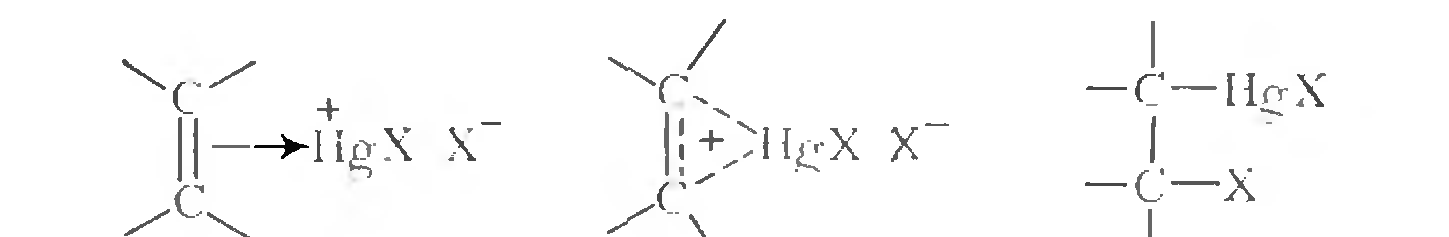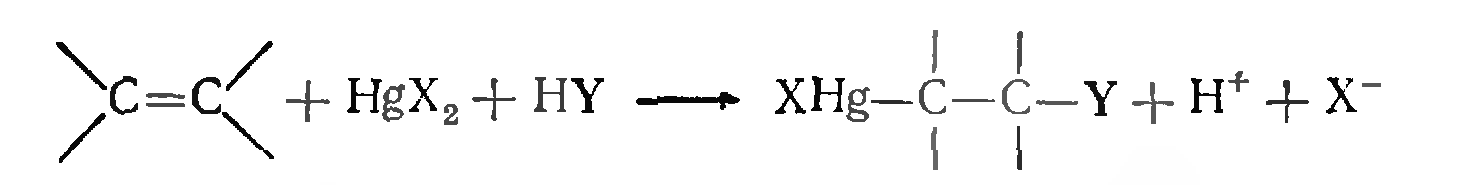Алкены чувствительны к электрофильной атаке солями ртути (II).
Ионы двухвалентной ртути, обладая большой электрофильностью, легко присоединяются к олефинам. При действии ацетата ртути (II) в водной среде в присутствии солюбилизаторов сначала образуется карбениевый ион, который в результате взаимодействия с водой дает продукт оксимеркурирования. Обычно его сразу восстанавливают до соответствующего спирта. Метод представляет собой ценный вариант гидратации алкенов (в особенности малореакционноспособных). Как правило, спирты образуются в соответствии с правилом Марковникова:
Меркурирование
Одним из наиболее важных общих методов построения связен углерод — ртуть является меркурирование, которое можно рассматривать как электрофильное присоединение ртутьорганнческих катионов к ненасыщенным системам.
Многие ароматические соединения способны вступать с солями ртути (II) в реакцию меркурирования, приводящую к арилзамещенным ртути (II) . В этой реакции могут быть использованы различные меркурирующис агенты. Обычно применяют раствор ацетата ртути(II) в уксусной кислоте; реакция катализируется хлорной кислотой. Меркурирование проявляет характерные черты реакций электрофильного ароматического замещения. Так, она протекает с большей скоростью, если ароматическое соединение содержит электронодонорный заместитель, давая в этом случае преимущественно орто и парамеркурированные продукты; вследствие большого размера атакующей частицы в продуктах часто преобладают паразамещенные. Если ароматическое соединение имеет электроноакцепторный заместитель, реакция идет в более жестких условиях, в этом случае в продуктах реакции повышается доля метаизомера. Ситуация, однако, осложняется тем, что реакция обратима, и вследствие этого состав се продуктов определяется термодинамическим контролем. На ориентацию могут оказывать влияние заместители, способные к координации.
Альтернативный метод введения группы Y состоит в добавлении к раствору соответствующего нуклеофильного реагента. Такие реакции «сольвомсркурироваиия» приводят к разнообразным ртутьорганическим соединениям, многие из которых являются удобными полупродуктами органического синтеза. Обычно реакции этого типа протекают как трансприсоединение, однако обратимость реакции может вести и к появлению некоторых количеств аддуктов. В некоторых случаях наблюдается цисприсоединение.
Взаимодействия этого типа являются промежуточными стадиями ряда важных реакций ненасыщенных соединений, катализируемых солями ртути. Многие из этих предполагаемых промежуточных продуктов были выделены, но относительно их строения в течение многих лет существовали разногласия; предполагали, что они могут быть симметричными комплексами, или аддуктами. В настоящее время твердо установлено (в частности, методами спектроскопии ЯМР), что эти соединения отвечают следующей структуре:
Хотя участие соединений других типов в качестве их предшественников вполне вероятно. При проведении реакций этого типа в протонсодержащих средах часто наблюдают внедрение в продукты реакции анионов растворителя.
Реакции ртутьорганических соединений
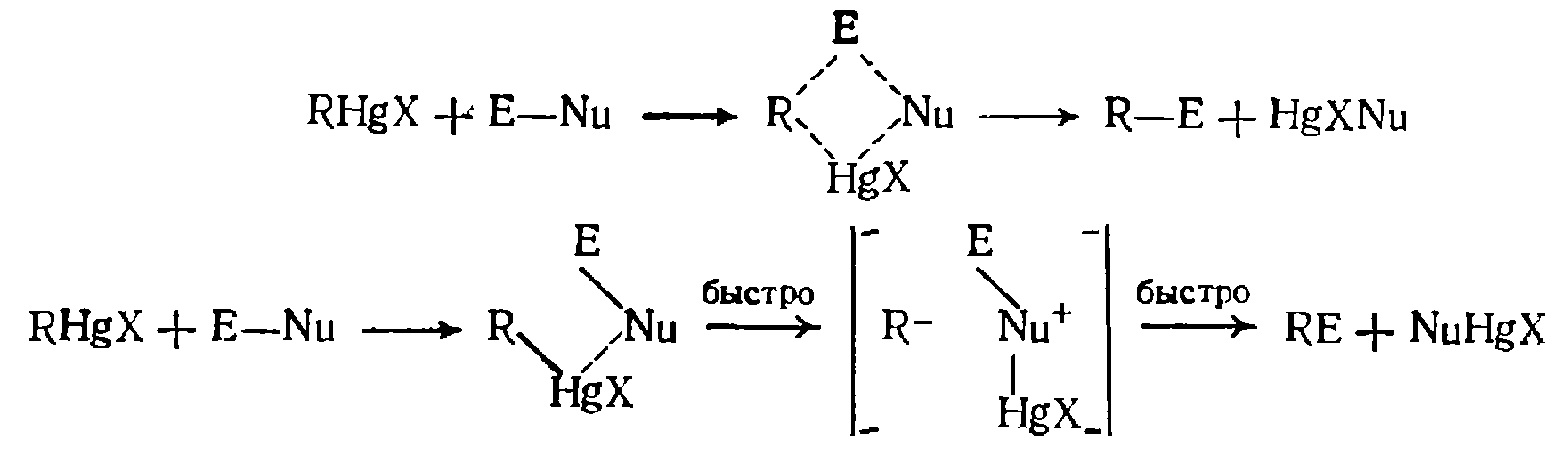
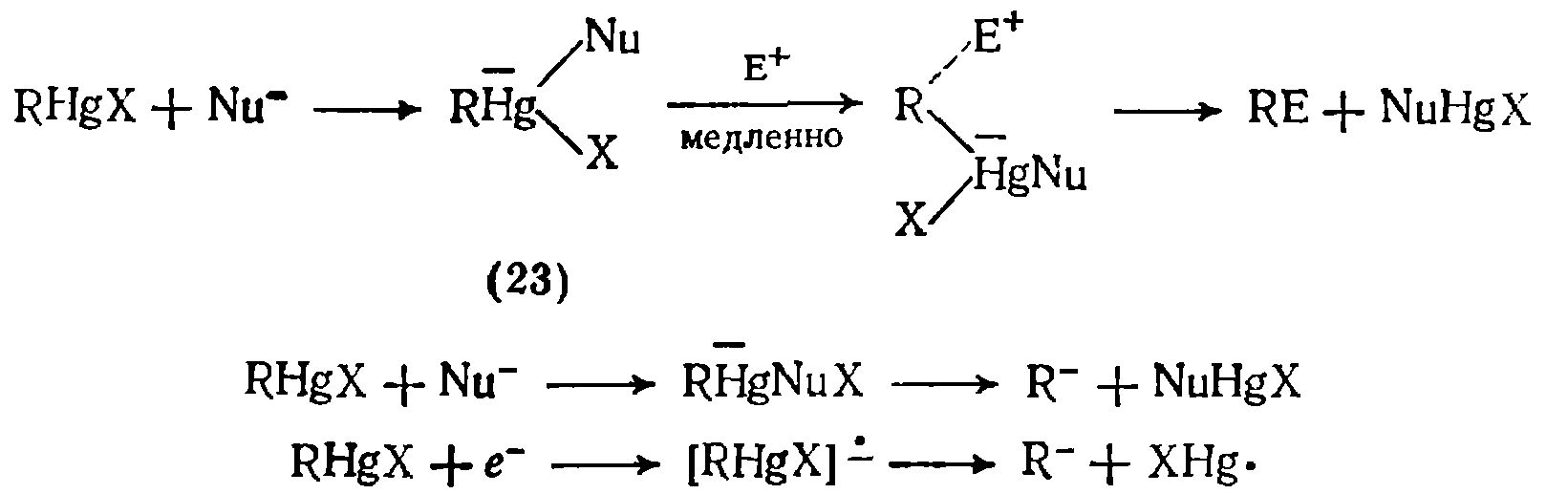
Простая, неассоциированная структура ртутьорганических соединений и обычная для них стабильность к гидролизу и окислению делают их удобными объектами для изучения механизмов реакции. Как было установлено, большинство электрофильных реакций ртутьорганических соединений имеют второй порядок, однако случаи прямого $Se_2$ механизма с инверсией конфигурации, подобной наблюдаемой для $Sn_2$ реакций, практически неизвестны. Вместо этого всегда наблюдается сохранение конфигурации, что указывает на механизм $Sei$. Обычно предполагают, что реакция протекает через четырехчленное циклическое переходное состояние, хотя возможно и ациклическое переходное состояние:
В ряде электрофильных реакций ртуть-органических соединений наблюдался нуклеофильный катализ; при этом, повидимому, образуются комплексы. Если электрофильная атака на промежуточное соединение является медленной стадией , реакция должна иметь второй порядок; в некоторых случаях, однако, эти реакции протекают по первому порядку. Поскольку образование карбаииона из ртутьорганического соединения маловероятно, следует полагать, что этот процесс осуществляется в условиях нуклеофильного катализа путем ионизации комплекса. Возможно также образование карбаниона при одноэлектронном переносе (нуклеофильный катализ сольватированным электроном ):
Связь углерод—ртуть является слабой, вследствие чего ртутьорганические соединения легко подвергаются термическим и фотохимическим гемолитическим реакциям. Иногда эти реакции наблюдались в качестве побочных процессов при электрофильном замещении. Следует отметить, что, как и для других диаллильных соединений металлов II группы, энергия активации гемолиза первой связи углерод — ртуть много больше, чем для второй связи.
Ртутьорганические соединения в синтезе
Применение ртутьорганических соединений в синтезе основывается на легкости, с которой ртуть может быть заменена на водород, алкильные пли различные функциональные группы. Реакции этого типа рассматриваются в зависимости от характера вводимого атома или группы. Эти реакции включают:
- Замена ртути на водород. Последовательность реакций сольвомеркурирование — демеркурирование представляет собой удобный общий метод присоединения к олефинам по правилу Марковникова. Стадия сольвомеркурирования была описана выше. Для проведения демеркуриро вания известно несколько методов, из которых наиболее часто применяют протолиз и восстановление гидридами металлов.
- Замена ртути на ацил (включая карбонилирование). Ацилирование ацилгалогенидами возможно в отсутствие катализаторов лишь для таких реакционноспособных ртутьорганических соединений, как меркурированные карбонильные соединения и некоторые гетероциклические производные ртути.
- Обмен ртути на галоген. Реакция ртутьорганических соединений с галогенами, приводящая к соответствующим галоген орган и чески м соединениям, является общим процессом и обычно протекает с высоким выходом.
- Замена ртути на кислород или серу. По отношению к кислороду ртутьорганические соединения весьма неактивны, хотя при продолжительном воздействии могут образоваться различные продукты. Озон же легко расщепляет ртутьорганические соединения. При этом из первичных алкилпроизводных в основном образуются карбоновые кислоты, хотя наблюдается также и интенсивная деградация органических остатков.
-
Реакции элиминирования ртутьорганических соединении:
- β Элиминирование с образованием алкенов. Во многих случаях удастся провести обращение реакции сольво меркурироваиия, т. с. возможны такие реакции, как, например, дезоксидемеркурированне. Такое элиминирование промотируется кислотами или сильнокоординирующими анионами (в частности, иодидионом). Реакция имеет трансстереохимию; в соответствии с кинетическими данными промежуточно образуются меркурииневые ионы.
- Карбеноидноеэлиминирование. Галогеналкилртутные соединения являются эффективными реагентами для получения циклопропанов из алкенов.
-
Ртутьорганические соединения в металлорганическом синтезе. Реакции металлов с соединениями диалкилртути представляют собой весьма общий, в некоторых случаях трудоемкий, метод получения органических соединений электроположительных металлов.