Полярный эффект
Если заместитель содержит заряженные частицы (положительные или отрицательные), то вокруг них образуется электрическое поле. Это поле действует на другие атомы по линии связей, а также непосредственно через пространство. В таком случае сила воздействия заместителя на другие частицы будет зависеть от конформации и конфигурации молекулы. Такое воздействие заместителя называют эффектом поля.
Эффект поля -- это взаимное влияние двух полярных групп в молекуле. При ионизации, в сильных электрических или магнитных полях, молекулы, имеющие связи $C-H$, показывают способность к сверхсопряжению.
Сверхсопряжение возникает, когда $\sigma $-электроны $C-H$-связей в возбужденном состоянии взаимодействуют с $\pi $-электронами ароматического ядра или соседней кратной связи.
На близком расстоянии эффект поля и индуктивный эффект заместителей нельзя отделять друг от друга, так как определить вклад каждого затруднительно. Обычно оба эффекта рассматривают вместе, а их общее влияние называют «полярным эффектом».
Если эффект поля обозначить $F$, а индуктивный эффект -- $I$, то можно наблюдать следующие эффекты:
- $+F(+I)$ -- эффект. Влияние считается положительным, если, заместитель по сравнению с водородом увеличивает электронную плотность по цепи атомов или уменьшает положительные заряды, находящиеся на ней и обусловленные наличием другой полярной группы.
- $-F(-I)$ -- эффект. Влияние -- отрицательное, если заместитель оттягивает на себя электроны, в результате чего атомы цепи приобретают положительный заряд или наблюдается снижение отрицательной заряженности цепи.
Влияние заместителя с увеличением расстояния падает благодаря проявлению им полярного эффекта. Заряд, возникающий при поляризации связей на атоме будет возбуждать меньшие заряды на соседних атомах.
Поляризация ковалентной связи со смещением электронной плотности наблюдается в пропилхлориде по сравнению с заряженностью атомов в пропане:
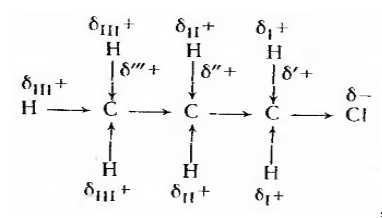
Рисунок 1.
где $\sum{{\sigma }^+}$=${\sigma }^-$; ${\sigma }^{`+} >{\sigma }^{``+} >{\sigma }^{```+} >$ ; ${\sigma }^+_I >{\sigma }^+_{II} >{\sigma }^+_{III} >$.
Регибридизация атома углерода -- одна из причин поляризации связей. При введении электроотрицательного заместителя увеличивается $p$-характер орбитали атома углерода, который образует связь с заместителем. При этом повышается орбитальная электроотрицательность, увеличивается полярность связей $C-C$ и $C-H$.
Для стабилизации карбаниона в илидах азота $R_3N-CR_2$, в которых отрицательно заряженный атом углерода расположен с положительно заряженным атомом азота, действует только эффект поля.
Илиды по своим свойствам более устойчивы, чем соответствующие им карбанионы.
Стабилизация карбанионов за счет эффекта поля происходит тогда, когда с реакционным центром связан какой -- нибудь гетероатом ($N, O, S$) и, если, хотя бы в одной из резонансных структур данный гетероатом несет положительный заряд:
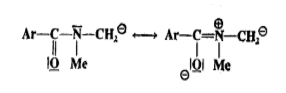
Рисунок 2.
Свойства полярного эффекта
Полярность связи, в большинстве случаев, будет возрастать с увеличением разности электроотрицательностей атомов, при этом индуктивный эффект и эффект поля изменяются параллельно.
Если между электроотрицательностью и эффектом поля нет корреляции, то полярный эффект изменяется параллельно с изменением эффекта поля.
Для оценки полярного эффекта можно использовать константы диссоциации замещенных уксусных кислот в водных растворах (данные по кислотно -- основным равновесиям):
$CH_3COOH + H_2O ↔ XCH_3COO^- + H_3O^+$
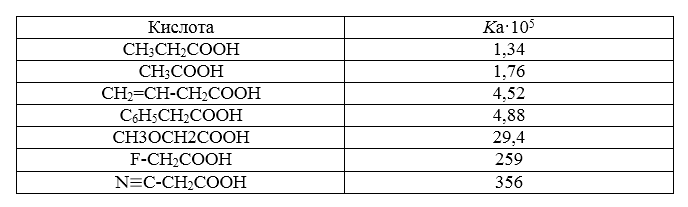
Рисунок 3.
Следовательно, заместители можно разместить по убывающему проявлению ими эффекта поля в ряд:
Так как группа $CH_3$- способна уменьшать константу диссоциации, ее относят к заместителям, проявляющим эффект поля.
Корреляция химических сдвигов с электроотрицательностью
Метод ядерного магнитного резонанса (ПМР-спектроскопия) позволяет оценивать относительные значения положительного заряда, который возникает на атомах углерода и водорода при смене заместителя $X$ в молекуле $CH_3X.$
Чем в более слабое поле смещен сигнал, тем более оттянуты с ядра валентные электроны, то есть, тем более оно дезэкранировано.
Между химическим сдвигом и электроотрицательностью существует хорошая корреляция:
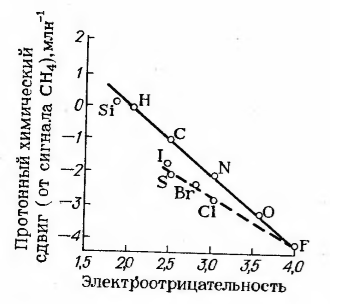
Рисунок 4.
Атомы галогенов ложатся на отдельную линию в результате влияния магнитной анизотропии связи $C-Hal$ на экранирование протона.
Генерируемый на протоне полложительный заряд находится в прямой зависимости от электроотрицательности заместителя, который проявляет полярный эффект.
- Заместители, имеющие атом, примыкающий к углеводородной цепи и находящийся в Периодической системе левее и ниже атома углерода $(B(CH_3)_2, Si(CH_3)_3$ и т.д.), проявляют положительный эффект поля.
- Положительно заряженные атомы проявляют более сильный положительный эффект поля, чем те же атомы в незаряженном состоянии: $N^+(CH_3)3 > N(CH_3)_2.$
- Отрицательно заряженные атомы будут проявлять эффект поля с противоположным знаком по сравнению с теми же атомами в незаряженном состоянии.
Группа $OH^-$ в спиртах $ROH$ проявляет отрицательный эффект поля, а заряженный отрицательно атом кислорода в анионах спиртов $RO$- проявляет положительный эффект поля.
У отрицательно заряженного атома положительный эффект поля тем больше, чем меньше заряд ядра атома.
По силе проявляемого ими эффекта атомы можно разместить в следующий ряд:
\[\equiv C^->=N^->-O^-\]При введении в молекулу, содержащую полярный заместитель, второго заместителя, наблюдается приближенная аддитивность их действия.











