Для насыщенных углеводородов характерна поворотная изомерия. Простая $\sigma $-связь не создает препятствий для вращения атомных группировок, которые окружают ее. Поэтому, например, в молекуле этана внутреннее вращение одной группы $-CH_3$ относительно второй не должно вызывать деформации $\sigma $- связи $C-C$ и может быть свободным. Опыты показывают, что при комнатной температуре это вращательное движение тормозится. Причиной торможения является взаимодействие не соединенных между собой атомов водорода в двух $CH_3$- группах, приводит к отталкиванию между этими атомами. Такой заторможен вращательное движение в молекулах этана и других углеводородов и их замещенных приводит к появлению поворотных изомеров.
Конформация
При вращении одной метательного группы в молекуле этана относительно второй вокруг углерод-углеродной связи атомы этих групп могут занимать в пространстве много различных взаимных положений. Это легко проследить на модели молекулы этана. Такие структуры молекулы характерны веществам с различным взаимным расположением атомов в пространстве. Они возникают при вращении вокруг простой углерод-углеродной связи, в отношении которой определяется положение атомов в пространстве. Это и называют конформациями (от лат. conformic - подобный), или поворотными изомерами (конформерами).
Конформации этана
Из большого количества конформаций этана можно выделить две крайние. Если вращать в пространстве одну $CH_3$-группу относительно второй и смотреть на модель этана вдоль $C-C$-связи, то можно заметить, что при одной из крайних конформаций атомы водорода одной $CH_3$-группы будут «заслонять», «затенять» атомы водорода второй $CH_3$-группы. Такую конформацию называют заслоненной, или затененной. При второй крайней конформации атомы водорода одной СН3-группы размещены в промежутках между атомами водорода второй $CH_3$-группы. Такую конформацию называют заторможенной (рис. 1).
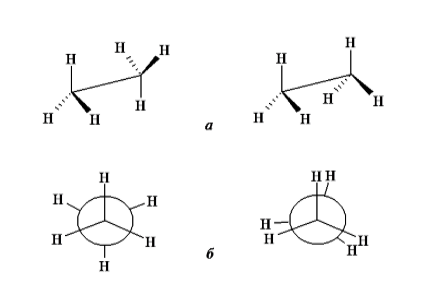
Рисунок 1. Перспективные формулы (а) и проекции Ньюмена (б) для заторможенной и заслоненной конформации этана
Для более наглядного изображения конформаций часто пользуются другой проекцией, где в центре, на пересечении трех прямых, находится атом углерода близкой к нам метательного группы. Связи $C-H$ второй метильной группы размещены по площади круга (на рис. 1 показаны штриховыми линиями). Такой способ изображения конформаций получил название формул Ньюмена.
Конформеры, изображены на рис. 1 отличаются друг от друга взаимным поворотом в пространстве $C-H$-связей одной метильной группы и $C-H$-связей второй метильной группы относительно связи $C-C$. Это взаимное их размещения в пространстве характеризует углом поворота $\varphi $.
Устойчивость конформаций
От обычных изомеров конформеры отличаются тем, что их, как правило, нельзя выделить в индивидуальном состоянии. Атомы в молекуле находятся в непрерывном движении и одна конформация легко переходит в другую. Конформации, которые возникают при свободном вращении вокруг $\sigma $-связей, имеют разную устойчивость. Как правило, молекула пытается приобрести такую конформацию, при которой ее потенциальная энергия была бы минимальной. Более энергетически выгодная, а потому и более устойчивая - заторможенная конформация, поскольку в ней атомы водорода одной метильной группы находятся на расстоянии от атомов водорода второй метильной группы, и поэтому взаимное отталкивание между ними будет минимальным. Запас внутренней энергии такой молекулы уменьшается. В связи с этим при таких положениях водородных атомов внутреннее вращение вокруг $C-C$-связи в какой-то степени тормозится. Отсюда и название конформации - заторможенная. Для перехода молекулы с заторможенной конформации в затененную необходимо затратить $12,6$ кДж / моль энергии.
Для этана переходы из заторможенной в заслоненную конформацию достигаются поворотом на $60^\circ$ относительно двух связей $C - H$:
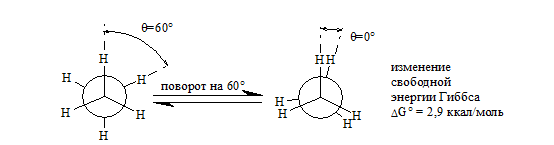
Рисунок 2.
Такой незначительный энергетический барьер, находится на уровне энергии теплового движения молекулы, не позволяет выделить отдельные поворотные изомеры, но существование их может быть зафиксировано некоторыми физическими методами, например, электронографическими, спектроскопическими и другими.
Конформации 1,2-дихлорэтана
При увеличении количества углеродных атомов в цепи возрастает количество возможных конформаций. Так, для бутана их уже шесть. Дизамещенные этана, например, 1,2-дихлорэтан, имеют конформаций больше, чем этан: транс-конформацию, две скошенные конформации и затененные конформации (рис. 3).
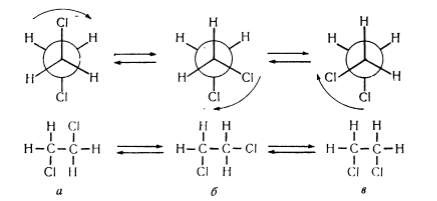
Рисунок 3. Конформации 1,2-ди-хлорэтана: а - транс-конформация; б, в - гош-конформации
В транс-конфорформации атомы хлора размещены в пространстве по разные стороны $C-C$-связи и отделены друг от друга (лат. trans - по ту сторону). Поэтому транс-конформация для дихлорэтана является энергетически выгодной и наиболее устойчивой. В скошенных конформациях атомы хлора расположены в пространстве ближе, чем в транс конформациях. Скошенные конформации, в которых двугранный угол между отдельными заместителями равен $60^\circ$, называют гош-конформациями (от старого французского слова, означающего «скручивание»), гош-конформации дихлорэтана менее устойчивы, чем его транс-конформации. Энергия молекулы дихлорэтана в гош-конформации больше от энергии гош-конформации на $5,9$ кДж / моль. Максимальную энергию его молекулы наблюдают в затененных конформациях (рис. 4).
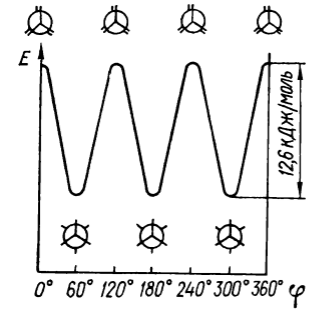
Рисунок 4. График зависимости потенциальной энергии Е от угла вращения $\varphi $ в молекуле этана
Конформеры дихлорэтана отличаются дипольными моментами. Так, транс-конформер неполярный, а гош-конформеры - полярные. В результате 1,2-дихлорэтан имеет средний дипольный момент ($1,27 \ D$ при $25^\circ \ C$) .При повышении температуры количество менее устойчивых гош-конформаций увеличивается и дипольный момент дихлорэтана повышается. При $315^\circ \ C$ он уже составляет $1,57 \ D$.
Конформации пропана
Для следующего гомолога, пропана, также имеется торсионное напряжение, возникающее в результате отталкивания двух пар атомов водорода (аналогично этану) и одного дополнительного взаимодействия между связями $C-H$ и $C-CH_3$ в заслоненной конформации:
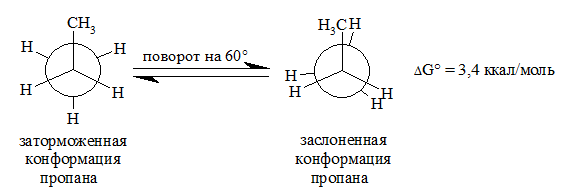
Рисунок 5.
Барьер вращения для пропана несколько выше, чем для этана, и составляет $3,4$ ккал / моль. Так как энергия каждого взаимодействия пары атомов водорода в заслоненной конформации составляет $1$ ккал / моль, энергия взаимодействия метильной группы и атома водорода в заслоненной конформации пропана и следующих гомологов алканов может быть оценена в $1,4$ ккал/моль.













