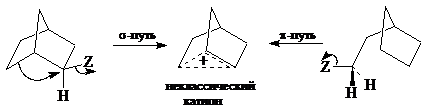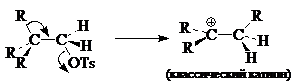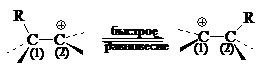Неклассическими карбокатионами назывются положительно заряженные частицы, в которых делокализация положительного заряда осуществляется с помощью многоцентровых МО, которые образуются за счет перекрывания атомных орбиталей по $\sigma$ - типу. Так аллильные катионы типа $CH_2=CHCH_{2^+}$ являются классическими, тогда как гомоаллильные катионы типа $CH_2=CH-CH_2CH_{2^+}$ в конформациях, в которых вакантные $p$-орбитали могут перекрываться с $\pi$-орбиталями, рассматриваются как неклассические:
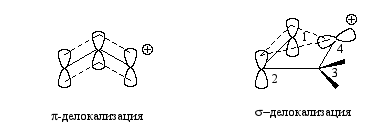
В аллильных катионах три взаимодействующие $p-AO$ перекрываются по $\pi$-типу, образуя делокализованную $\pi$-систему, тогда как в гомоаллильных катионах осуществляются перекрывания $\sigma$-типа, поскольку вакантные $p$-орбитали на $C$(4) взаимодействуют с $p$-орбиталями на $C$(1) и $C$(2) лишь одной своей долей. Наличие $pi$-связей между $C$(1) и $C$(2) принципиально неважно, так как вакантные орбитали локализованы лишь с одной стороны плоскости двойной связи, что обусловливает различие в симметрии между аллильными и гомоаллильными ионами. Аллильные катионы имеют $\pi$-симметрию, тогда как гомоаллильные — $\sigma$-симметрию. На схеме 1 приведены примеры классических и неклассических структур карбокатионов.

В формулах неклассических ионов пунктирными линиями обозначают многоцентровые (обычно трехцентровые связи), а сплошными линиями - нормальные классические двухэлектронные $\sigma$-связи.
Неклассические катионы можно получать в сольволитических реакциях путем отщепления уходящих групп с участием или соседних $\pi$-связей ($\pi$-путь), или соседних $\sigma$-связей ($\sigma$-путь), например:
Однако сам факт участия соседних групп не обязательно указывает на образование неклассического карбокатиона, так как анхимерное содействие может приводить и к классическим катионам:
Доказать образование неклассических ионов чрезвычайно трудно, так как всегда существует альтернативные объяснения экспериментальных данных не через неклассические карбокатионы, а через очень быстрое равновесие между двумя классическими структурами:
При быстром переходе групп $R$ от $C$(1) и $C$(2) свойства этих атомов углерода усредняются, и получается картина, неотличимая от той, которая наблюдалась бы в случае неклассического иона. В очень быстрой равновесной изомеризации классических структур ион с неклассической структурой может являться или очень короткоживущим интермедиатом, или переходным состоянием.
Арилдиазониевые катионы
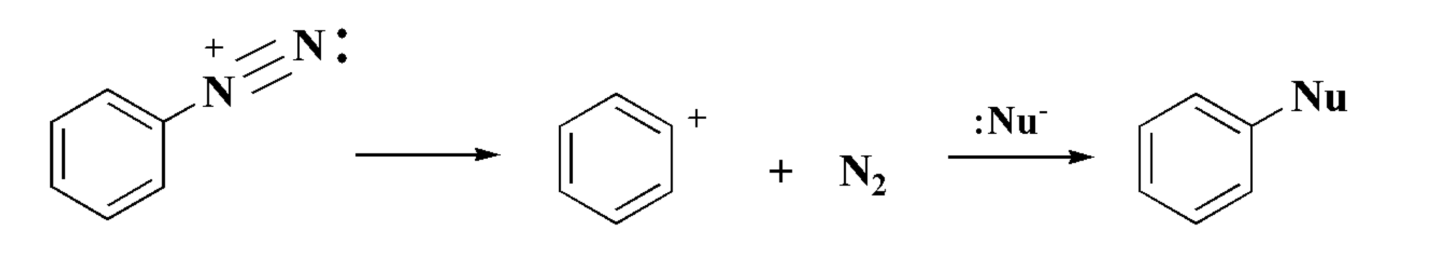
Одними из самых употребляемых промежуточных частиц при нуклеофильном ароматическом замещении является арилдиазониевые соли. Обычно они готовятся реакцией анилина с азотистой кислотой, генерируемый при реакции (in situ) с натрий или калий нитритом. В противоположность алкилдиазониевим солям быстро разлагаются на молекулярный азот и карбокатион и продукты его превращения, ариздиазониевые соли достаточно устойчивы в растворе при температуре $0-5^\circ C$. Они также могут быть выделены в виде солей с такими ненуклеофильнимы анионами, как тетрафтороборат или трифтороацетат. Образование диазоний-иона происходит через стадии присоединения нитрозоний-катиона к аминогруппе и последующего отщепления молекулы воды.
Наибольшая ценность арилдиазониевых солей как синтетических промежуточных частиц объясняется наличием удобной отходящей группы - молекулярного азота $N_2$.
Механизмы замещения уходящей группы в арилдиазониевых катионах
Существует три основных механизма, по которым происходит замещение -$N_2$.
-
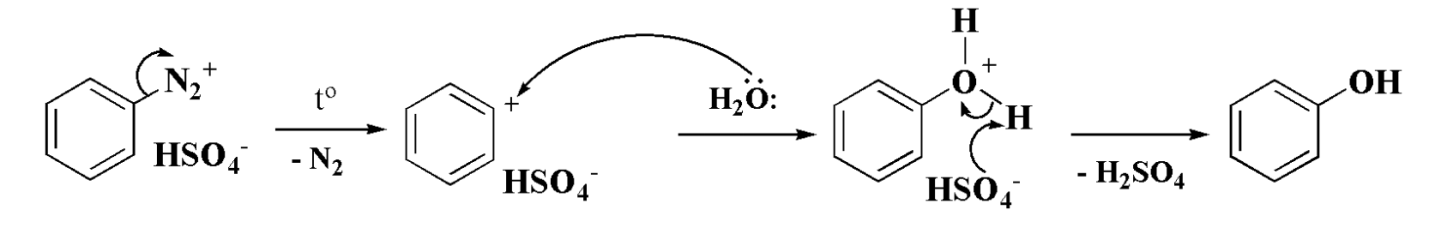
Первый включает внутримолекулярное термическое разложение диазониевого иона с образованием арильного катиона, что увлекается нуклеофилом. Арильный (фенильный) катион очень нестабилен, поэтому он не является селективным, здесь нуклеофилом может быть как анион, так и молекула растворителя.
Примером такого типа механизма является гидролиз соли диазония с образованием фенолов. Для превращения в фенолы арилдиазониеви соли нагревают с водой. В этих условиях вероятно образование фенильного катиона:
При этом возможна реакция с другими нуклеофилами, находящихся в реакционной среде, например, галогенид-анионами. Чтобы предотвратить это, как противоион можно использовать гидрогенсульфат-анион $HSO_{4^-}.$
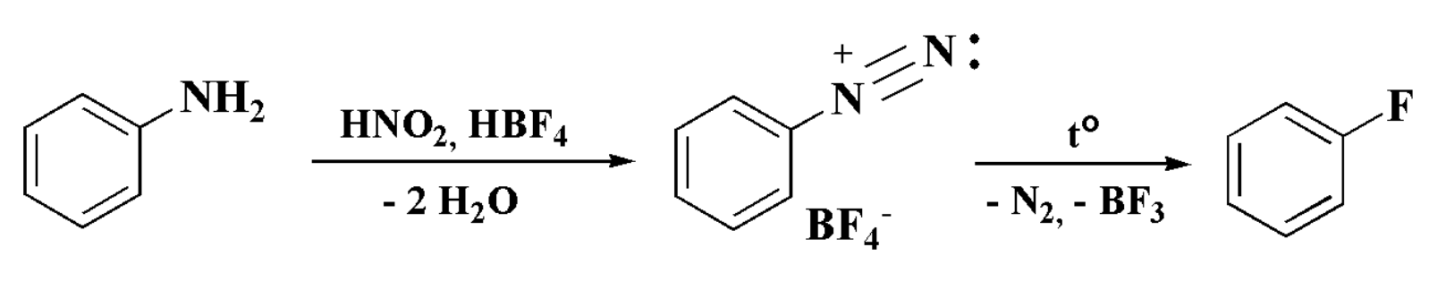
Через ион диазония можно ввести атом фтора. Один из методов заключается в выделении тетрафлуороборатив диазония и их термическом разложении с образованием фторзамищеных бензола (реакция Шимана). Считают, что такая реакция происходит из-за образования фенильного катиона, что забирает атом фтора с тетрафлуороборатного аниона:
Диазоний тетрафторобораты можно приготовить осаждением из водного раствора с помощью тетрафлуороборатнои кислоты или диазотировании гарега-бутилнитритом и трифлуоридом бора по безводных условиях в таких органических растворителях, как эфир, тетрагидрофуран, ацетонитрил. Для этой же цели можно использовать гексафлуорофосфатни соли диазония.
-
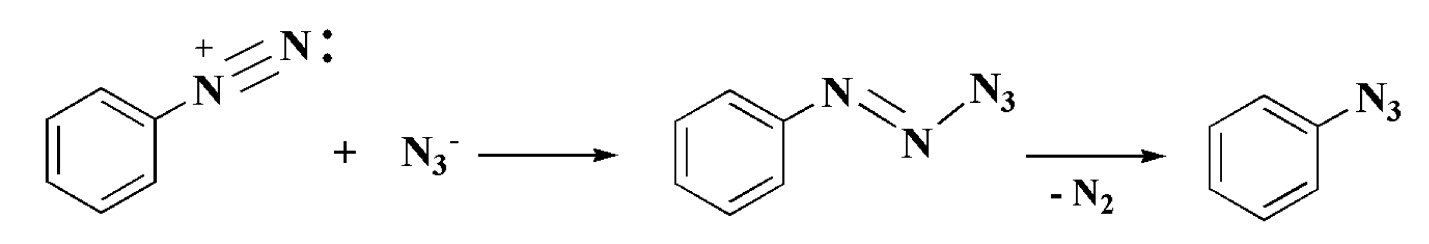
Вторым возможным механизмом замещения может быть образование аддукта соли арилдиазония с нуклеофилом и его разложение с потерей азота. Так происходит реакция с азид-ионами с образованием арилазидов:
Аналогично происходит образование йодобензена.
-
Третий механизм включает окислительно-восстановительный процесс, и он характерен для реакций, в которых в качестве катализаторов применяются соли меди ($I$). По реакции с галогенидами меди ($I$) можно получить арилхлориды или арилбромиды (реакция Зандмайера).