Ядерный магнитный резонанс
Метод ядерного магнитного резонанса (ЯМР) часто используется для определения оптической чистоты. Этот метод основан на применении оптически активных растворителей, в которых химические сдвиги дают энантиотопные атомы, содержащиеся в оптических антиподах.
Так, методом ЯМР определили оптическую чистоту 2,2,2-трифтор-1-фенилэтанола с применением (+)-$\alpha$-фенилэтиламина в качестве растворителя, оптическую чистоту метиловых эфиров $\alpha$-аминокислот и аминов с применением в качестве растворителя (-)-2,2,2-трифтор-1-фенилэтанола.
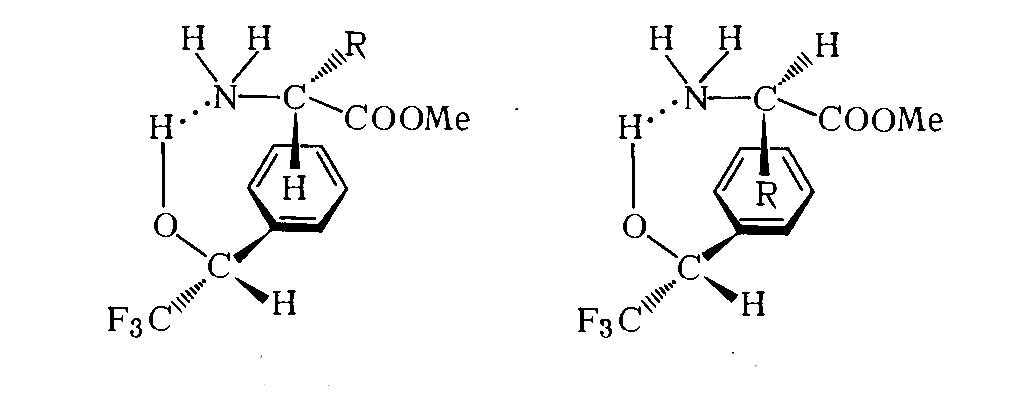
Отличительные особенности в химических сдвигах зависят от образования диастереомерных сольватов. При взаимодействии антиподных метиловых эфиров $\alpha$-аминокислот с 2,2,2-трифтор-1-фенилэтанолом появляются диастереомерные сольваты (А) и (Б). Их наличие обусловлено взаимодействием атома водорода гидроксила с атомом азота аминогруппы и π-электронного облака ароматического ядра с углеродным атомом карбоксигруппы.
Условия образования сольвата в соединении (А) выгоднее, чем сольвата (Б), так как в случае (Б) взаимодействию ядра и углеродного атома карбоксигруппы препятствует радикал аминокислоты, который повернут в сторону ядра.
Рисунок 1.
Подобным образом можно определять оптическую плотность спиртов.
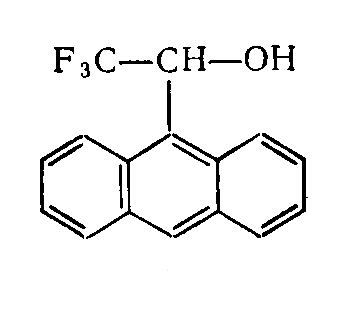
Достойным хиральным сольватирующим агентом является (-)-2,2,2-трифтор-1-(антрил-9)этанол
Рисунок 2.
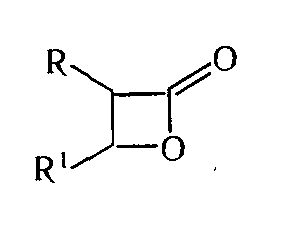
С помощью этого реагента определили оптическую чистоту $\beta$-пропиолактона и его аналогов
Рисунок 3.
Кроме спектроскопии ЯМР $1H$ для нахождения энантиомерной чистоты применяют и ЯМР на других ядрах.
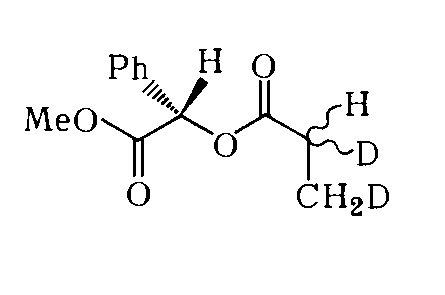
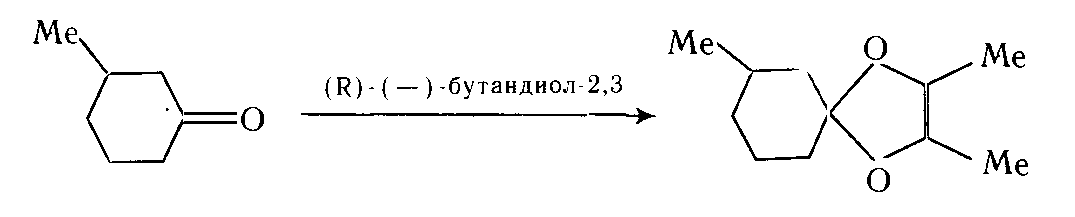
Например, для соединений с дейтериево – водородной асимметрией $CH_2 D-C^* HD-COOH$ и $CH_2 D-C^* HD-NH_2$, которые получили из алкенов дейтерированием в присутствии $RH-DIOP$, использовали спектроскопию ЯМР $2H$ после превращения в диастереомеры
Рисунок 4.
действием соответственно (S)-метилового эфира миндальной кислоты и (-)-камфаноилхлорида.
Рисунок 5.
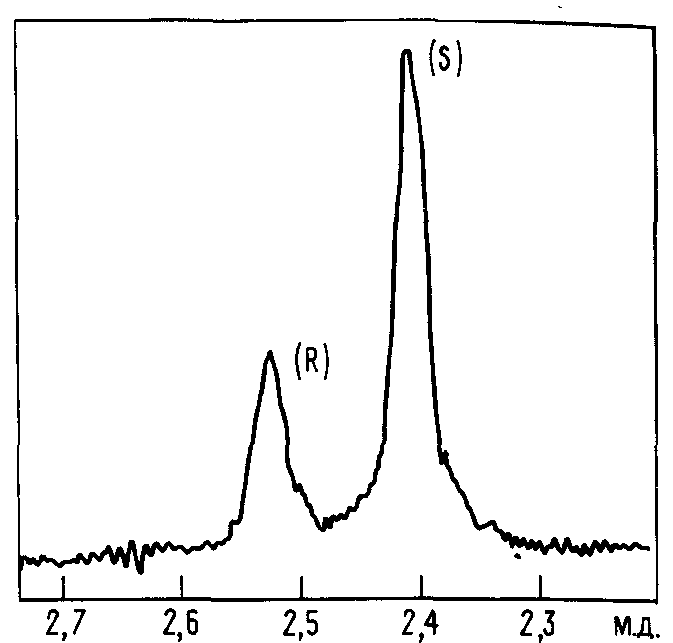
Спектры ЯМР $2H$ (в бензоле) диастереомеров с дейтериево – водородной асимметрией
Методом спектроскопии ЯМР $13C$ в твердой фазе можно различать рацемат и оптически активную винную кислоту. Сигналы $13C$ будут различны в результате разного размещения молекул в кристаллах оптически активного рацемата и соединения.
Комплексное сочетание методов определения оптической чистоты
Иногда для нахождения энантиомерной чистоты необходимо применять комплексное использование нескольких методов. Например, для установления энантиомерной чистоты менее 1% у хиральных вторичных спиртов применяют методику, сочетающую ГЖХ (или ЯМР), ацидиметрическое титрование и поляриметрическое измерение.
Предложен метод измерения энантиомерной чистоты без применения вспомогательного оптически активного вещества и без знания величины максимального оптического вращения.
Для этого вещество $R^*H$, оптическую чистоту которого нужно узнать, переводят в производное с двумя связанными остатками $R^*$; для спиртов и аминов это могут быть эфиры или амиды с дикарбоновыми кислотами, а для аминокислот – дипептиды.
Если соединение $R^*H$ не было оптически чистым, то появляются два диастереомера - мезо- и $DL$-формы:
$R_R^* H+R_S^* H→R_R^* H-R_S^* H+(R_R^* H-R_R^* H+R_S^* H-R_S^* H)$
Соотношение мезо- и $DL$-формы определяют для реакции с рацемическим, а после с оптически активным исходным $R^*H$, в этом случае - с различной глубиной превращения. Найденные значения применяют для расчета энантиомерной чистоты $R^*H.$
Если проводится анализ веществ , которые дают хроматограммы со значительными перекрывающимися пиками, то проводят параллельные измерения спектров поглощения и оптического вращения отдельных фракций. Эти данные также применяют для расчета энантиомерной чистоты.
Для нахождения энантиомерной чистоты иногда применяют круговую поляризацию люминисценции. Этот метод применяется при малой энантиомерной чистоте.
Определение энантиомерной чистоты гликолей
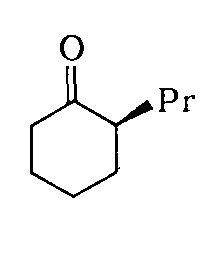
Для определения оптической чистоты гликолей осуществляют их перевод в ацетали в результате взаимодействия с ($S$)-(+)-2-пропилциклогексаном:
Рисунок 6.
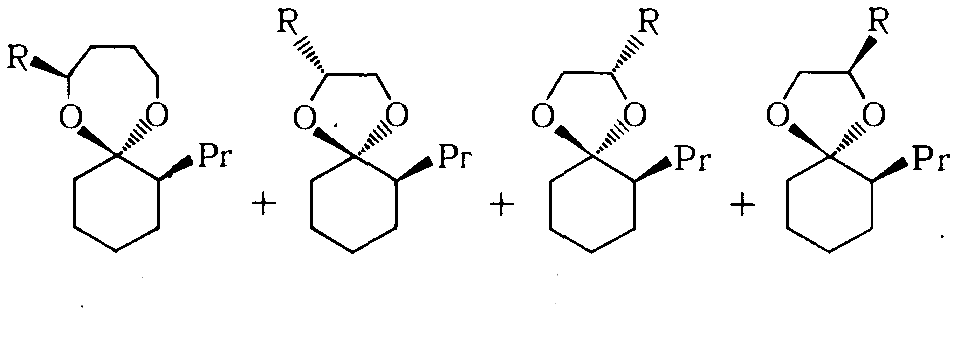
При этом атом углерода карбонильной группы превращается в дополнительный хиральный ценр, в результате чего возникает четыре диастереомера.
Рисунок 7.
В HPLC и спектрах ЯМР $13C$ все эти диастереомеры дают раздельные сигналы , причем площади сигналов для первого и второго диастереомера ( как и для третьего и четвертого) одинаковы в случае рацемических гликолей. В случае оптически активных гликолей соотношение этих площадей позволяет определять оптическую чистоту.
Если 2-пропилциклогексанон заменить бензальдегидом, то также образуется четыре ацеталя:
Рисунок 8.
В зависимости от положения фенильной группы относительно остатка R появляются два $σ$-диастереомера – цис- и транс-, каждый из которых дает свой сигнал бензильного протона в спектре ПМР. Каждый из сигналов является суммой двух диастереомеров, которые различаются конфигурацией остатка гликоля.