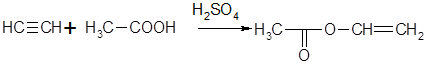Общие сведения о реакциях электрофильного присоединения
Реакции электрофильного присоединения — реакции присоединения, в которых атаку кратной связи в начальный момент взаимодействия осуществляет электрофил, т.е. положительно заряженная частица или частица с дефицитом электронов. В органической химии чаще всего в роли атакующей электрофильной частицы выступает протон $H+$. Образующийся на конечной стадии взаимодействия карбокатион подвергается нуклеофильной атаке.
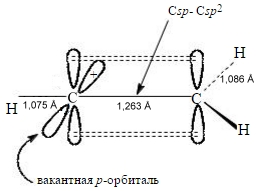
Реакции электрофильного присоединения весьма распространены среди непредельных углеводородов и широко используются в промышленном химическом производстве и лабораторных синтезах. При этом скорость реакций электрофильного присоединения для алкенов и алкинов различна. Это связано, во-первых, с тем, что высшие занятые молекулярные орбитали (ВЗМО) у алкинов располагаются ниже, чем у алкенов. Во-вторых, стабильность интермедиатов, образующихся в ходе электрофильного присоединения к соединениям указанных классов непредельных углеводородов различна. В первом случае образуется карбокатион, во втором случае –винил-катион. При этом центральный атом углерода находится в $sp$-гибридном состоянии, в то время как вакантная $p$-орбиталь располагается перпендикулярно $\pi$-связи. Поскольку атом углерода винил-катиона в $sp$-гибридизации обладает более высокой электроотрицательностью по сравнению с углеродным атомом алкил-катиона в $sp_2$- гибридизации, винил-катион менее стабилен, чем алкил-катион:
Отсюда следует, что алкины менее склонны к участию в реакциях электрофильного присоединения, чем алкены и лишь присоединение кислотных агентов и воды к тройной и двойной связям происходит с близкими скоростями.
Присоединение галогеноводородов
В общем случае при гидрогалогенировании алкинов реакция идет по правилу Марковникова, т.е. атом водорода присоединяется к наиболее гидрогенизированному углеродному атому кратной связи:
$CH\equiv C-CH_3+HCl{{\stackrel{влага}{\longrightarrow}CH_2=CCl-CH_3}}$
Однако при дальнейшем гидрогалогенировании до соответствующего алкана присоединение галогеноводорода к кратной связи идет уже против правила Марковникова:
$CH_2=CCl-CH_3+HCl{{\stackrel{влага}{\longrightarrow}Cl-CH_2-CHCl-CH_3}}$
Возможны два механизма протекания реакции гидрогалогенирования алкинов: бимолекулярный $Ad_E2$ и тримолекулярный $Ad_E3.$
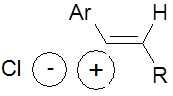
В первом случае в качестве интермедиата образуется открытый винил-катион, связанный с галогенид-ионом:
При дальнейшем взаимодействии винил-катиона с галогенид-ионом или с растворителем образуется смесь цис- и транс-изомеров винилгалогенидов.
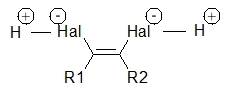
Во втором случае электрофил и нуклеофил из разных молекул галогеноводорода атакуют разные атомы углерода кратной связи с образованием интермедиата, включающего две молекулы галогеноводорода и одну молекулу алкина:
Присоединение кислот
В случае присоединения сильных неорганических кислот к алкинам образуются очень слабые нуклеофилы, поэтому для такого рода взаимодействий реализуется только бимолекулярный механизм электрофильного присоединения.
Карбоновые кислоты также способны электрофильно присоединяться молекулам алкинов. Эти реакции катализируются солями ртути и протекают в соответствии с правилом Марковникова. В результате в зависимости от условий образуются либо енолацетаты, либо геминальные диэфиры (в случае присоединения двух молей кислоты). Например, в результате взаимодействия ацетилена с уксусной кислотой получается винилацетат:
Присоединение галогенов
В ходе галогенирования алкинов атомы галогена последовательно присоединяются к атомам углерода, участвующим в образовании кратной связи:
$CH\equiv CH+Cl_2{{\stackrel{H_2O}{\longrightarrow}}}CHCl=CHCl$
$CHCl=CHCl+Cl_2{{\stackrel{H_2O}{\longrightarrow}}}CHCl_2-CHCl_2$
Или в случае избытка галогена:
$CH\equiv CH+2Cl_2{{\stackrel{H_2O}{\longrightarrow}}}CHCl_2-CHCl_2$
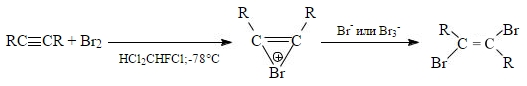
В первом случае образуется в основном транс-изомер, что связано с образованием галогенирениевого иона в качестве интермедиата. Например, в случае бромирования образуется бромирениевый катион:
В целом можно заключить, что моноалкилацетилены и фенилацетилены присоединяют галоген по $Ad_E2$-механизму через открытый винил-катион, связанный с галогенид-ионом в форме контактной (тесной) ионной пары.
Гидратация алкинов
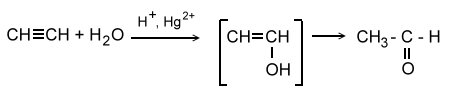
В результате гидратации ацетилена образуется ацетальдегид (реакция Кучерова):
При этом в качестве промежуточного продукта образуется енол – непредельный спирт, содержащий годроксильную группу при двойной связи.
Присоединение воды к тройной связи протекает по правилу Марковникова, поэтому при гидратации как терминальных, так и нетерминальных алкинов всегда образуется соответствующий кетон.
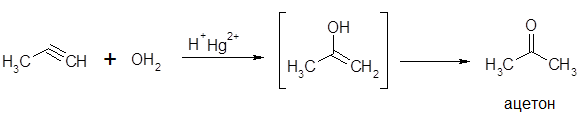
Например, в результате гидратации пропина образуется ацетон:
Помимо солей ртути гидратацию алкинов катализируют соли золота (III), меди (I), серебра и рутения (III).
Присоединение сульфогалогенидов и селенгалогенидов
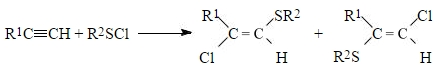
Присоединение сульфогалогенидов к алкинам происходит исключительно по принципу анти-присоединения и приводит к образованию двух продуктов, один из которых образуется по правилу Марковникова, а другой – против правила Марковникова:
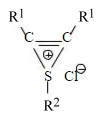
При этом разница во взаимодействии с терминальным и нетерминальным алкином заключается лишь в различии скорости протекания реакции: в случае нетерминального алкина реакция идет быстрее благодаря образованию циклического катионного интермедиата:
Аналогичным образом протекают реакции с участием селенгалогенидов с той лишь разницей, что «центральным» атомом циклического катионного интермедиата является селен.
Присоединение солей ацилия
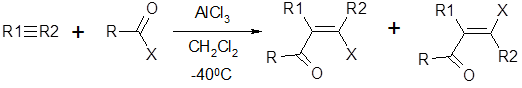
Взаимодействие алкинов с ацилгалогенидами происходит в присутствии хлорида алюминия в хлористом метилене. При этом образуется смесь цис- и транс-хлорвинилкетонов:
При этом электронодонорные заместители в радикале ацилгалогенида способствуют транс-присоединению, электроноакцепторные - цис-присоединению.