Поляриметрия
Под оптической активностью понимают способность растворов, паров веществ, кристаллов вызывать вращение плоскости поляризации проходящего через данную среду оптического излучения.
Оптически активные вещества делят на правовращающие (вращающие положительно) и левовращающие (вращающие отрицательно) виды. Разновидность зависит от поворота плоскости поляризации (по или против часовой стрелки, если смотреть навстречу ходу лучей света).
Вращающая способность вещества зависит от длины волны излучения и от температуры. При определении оптической активности вещества используют монохроматическое излучение при постоянной температуре.
Величина, зависящая от угла φ, определенного на поляриметре, длины l (в дециметрах) пропускающего слоя вещества, называют удельным вращением [α].
$φ=[α] \cdot l \cdot C,$
где $C$ – концентрация оптически активного вещества.
Удельное вращение представляет собой угол, на который 1 г вещества в 1 мл жидкости отклоняет плоскость поляризации света при длине пропускающего слоя, равной 1 дм.
Часто удельное вращение изменяется с природой растворителя.
В одном и том же растворителе удельное вращение не всегда меняется пропорционально концентрации в результате явлений сольватации, ассоциации, ионизации.
Принцип свободного вращения
Два атома, связанные между собой простой связью, согласно классической стереохимии, свободно вращаются вместе с заместителями вокруг общей связи.

Принцип свободного вращения подходит не для всех соединений. Известны вещества, в которых свободное вращение относительно общей связи заторможено, что приводит к возникновению оптически активных изомеров.
Существуют соединения, в которых в определенных положениях вращение затруднено, то есть является ограниченным вращением.
Молекулярная асимметрия – условие оптической активности
Еще Пастер установил, что только вещества, обладающие асимметрическим строением, будут оптически активными. Молекула является асимметричной, если при любом вращении она не совпадает со своим зеркальным отражением.
Молекула является асимметричной, если не обладает плоскостью и центром симметрии. Оптические изомеры отличаются расположением атомов и групп атомов в трехмерном пространстве.
В молекуле, содержащей два асимметричных атома углерода, каждый атом сохраняет свою индивидуальность. В таком случае наблюдаемый эффект является суммой действия каждого атома.
Например: В алкалоиде эфедрине оба асимметричных атома могут быть поочередно правовращающими или левовращающими. Следовательно, возможны конфигурации:
- +, +;
- -, -;
- +, -;
- -, +

В случае 1,2, когда оба симметричных атома правовращающие или левовращающие, их действие суммируется. В первом случае молекула будет правовращающей, во втором – левовращающей. Если же атомы имеют разные направления вращения, то оптичекая активность будет разностью активностей этих двух атомов.
Следовательно, молекула с двумя асимметричными атомами может обладать четырьмя оптически активными формами. Существуют две рацемические смеси с разными физическими свойствами.
Формы 1 и 2 не будут оптическими антиподамидля форм 3 и 4, они не относятся друг к другу как предметы к своему зеркальному отражению. Изомеры 1 и 2 являются диастереоизомерами форм 3 и 4.
Число оптических изомеров молекул, которые содержат n асимметричных атомов, равно 2n.
Например: Молекула, имеющая три асимметричных атома будет обладать 23=8 изомерами (четыре пары антиподов), молекула с четырьмя асимметричнымиатомами – 16 изомерами или 8 парами антиподов и т.д.
Внутримолекулярная компенсация
Иногда, оба асимметричных атома в молекуле обладают тождественным строением, то есть каждый из асимметричных атомов замещен одинаковыми группами.
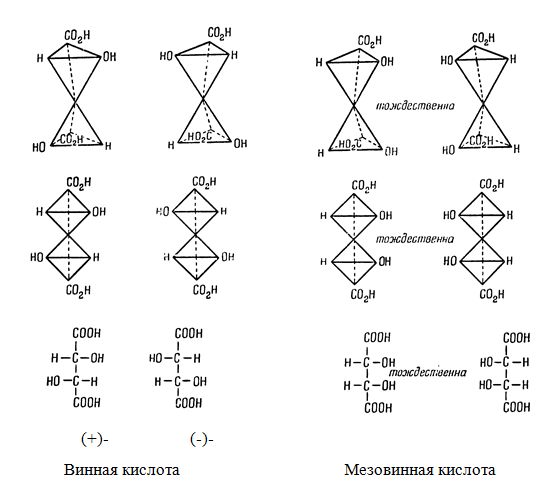
Например: Винная кислота $HOOC-CHOH-CHOH-COOH$. Строение обоих атомов одинаково и они обладают одинаковой вращающей способностью. Изомеры (+, +) и (-, -) являются правовращающим и левовращающим соответственно. В изомерах (+, -) и (-, +) направление вращения противоположно при одинаковом вращении. Поэтому действие этих асимметрических атомов взаимно компенсируется. Оба изомера являются в действительности одним веществом, поэтому оно неактивно вследствие внутримолекулярной компенсации.
Таким образом, винная кислота имеет два оптических антипода (+, +) и (-, -), один неактивный изомер – мезовинную кислоту и рацемическую форму – рацемическую (виноградную) кислоту.
Неактивные вследствие внутримолекулярной компенсации изомеры отличаются от неактивных рацемических форм тем, что их нельзя расщепить на оптические антиподы.
Для изображения винных кислот и аналогичных соединений пользуются:
- перспективными конфигурационными формулами;
- схематическими конфигурационными формулами;
- проекционными формулами.
Конфигурационные формулы (+), (-) винных кислот не имеют плоскости симметрии. Так как они в пространстве несовместимы ни при каких вращениях, то представляют собой два оптических антипода.
Молекула мезовинной кислоты обладает плоскостью симметрии, а при определенном положении тетраэдров относительно друг друга, и центром симметрии. Поэтому данное соединение оптически неактивное.