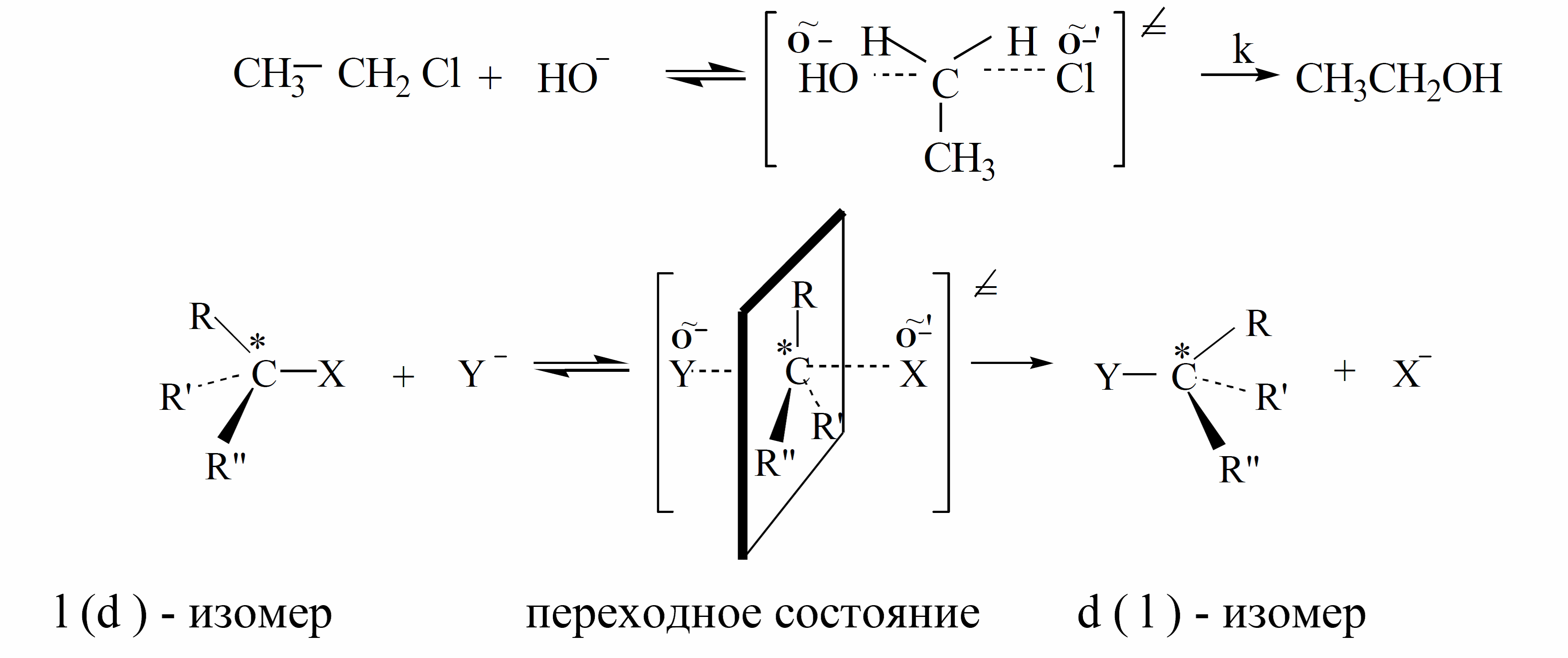
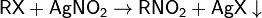Бимолекулярное нуклеофильное замещение $S_N2$ это одностадийный процесс, протекающий через переходное состояние (активированный комплекс):
В исходном состоянии атом углерода, где происходит замещение, находится в состоянии $sp^3$ - гибридизации. Нуклеофильный реагент атакует положительный центр субстрата с электростатически наиболее выгодной «тыльной стороны», так как в этом случае на него не действует одноименный заряд атома $X$. Наименьшая энергия требуется при атаке атома углерода по прямой, соединяющей центр атомов $C$ и $X$. Момент, когда старая связь не разорвалась, а новая еще не образовалась, соответствует переходному состоянию. Центральный атом при этом находится в состоянии, близком к $sp^2$ - гибридизации.
Для достижения такого состояния требуется затрата энергии (энергия активации), поэтому переходному состоянию соответствует максимум энергии.
При дальнейшем превращении активированного комплекса в конечный продукт, снова происходит изменение гибридизации углеродного атома. Он имеет $sp^3$ - гибридизацию. Таким образом, реакция протекает с полным обращением конфигурации при реакционном центре.
Стереохимия процесса
При использовании оптически активного соединения после проведения реакции по $S_N2$ - механизму происходит инверсия (обращение) молекулы и образование оптического антипода. Здесь имеет место еальденоеское обращение.
Если подход со стороны, противоположной уходящей группе, невозможен вследствие особенностей реагирующих систем, например, полициклических соединений с уходящей группой в голове моста, то реакция $S_N2$ становится невозможной.
В процессе реакции происходит изменение сольватации: уменьшается сольватация нуклеофила, так как уменьшается отрицательный заряд на нем, и увеличивается сольватация уходящей группы. Кроме того, при движении системы к активированному комплексу увеличивается роль дисперсионной сольватации, так как активированный комплекс более поляризован, чем исходное и конечное состояния.
Кинетика $S_N2$ процесса
Так как нуклеофил участвует в образовании переходного состояния, скорость реакции зависит как от природы, так и от концентрации нуклеофила. Кинетика $S_N2$ - процесса описывается уравнением второго порядка:
$r = k [ R X ] [ Y ]$
В тех случаях, когда в качестве нуклеофила используется молекула растворителя и концентрация нуклеофила практически не изменяется в процессе реакции, реакция может описываться уравнением первого порядка:
$r = k [Sol] [RX] = k'[RX]$.
Но реакция по-прежнему остается бимолекулярной, так как молекула растворителя включена в переходное состояние и происходит образование ковалентной связи.
Характеристика и примеры реакций проходящих по $S_N2$ механизму
К этому типу реакций относятся реакции нуклеофильного замещения, которые проходят по связи $C-Hal$ по общей схеме:
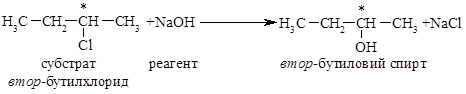
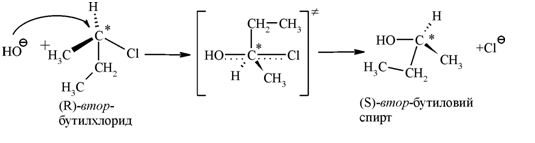
Для первичных и вторичных галогенпроизводных углеводородов механизм этой реакции следующий:
Нуклеофил $OH$-группа атакует асимметричный атом углерода ($C*$- электрофильный центр) с противоположной относительно галогена стороны с образованием плоского переходного состояния (ПС), который стабилизируется отщеплением галогенид-аниона. В приведенном примере замещение хлора происходит у асимметричного атома углерода, поэтому в ходе реакции происходит вращение конфигурации молекулы (Вальденивське вращения; Вальден, 1896 г.), которое уже рассматривалось ранее.
Реакция бимолекулярна, то есть скорость зависит как от концентрации субстрата так и реагента. Скорость этой реакции соответствует реакции второго порядка: $V = k\cdot [CH_3CH_2CH(Cl)CH_3] [OH^–]$.
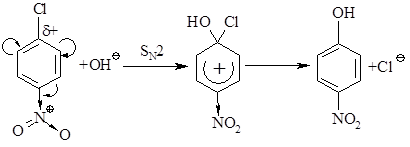
К этому же типу реакций относятся реакции нуклеофильное замещение галогена, связанного с ароматическим ядром:
Реакция идет по $S_N2$ механизму, при этом роль сильного акцептора электронов, например, $NO_2$ заключается в увеличении положительного заряда $\delta+$ на атоме углерода, непосредственно связанном с галогеном.
Также по $S_N2$ механизму протекает широко известная реакция Мейера - получение алифатических нитросоединений реакцией алкилгалогенида и нитрита серебра.
По $S_N2$ механизму протекает множество других реакций.
Зависимость $S_N2$ нуклеофильного замещения от внешних факторов
В этих реакциях $S_N2$ нуклеофильное замещение зависит от ряда факторов:
-
Структуры субстрата (в данном случае галогеналкана). Так для первичных галогенпроизводных углеводородов ($R Hal$) характерен $S_N2$-механизм для вторичных и третичных $S_N1$.
Ряд реакционной способности субстратов в реакциях $S_N2$:
$PhCH_2X > EWG–CH_2X > CH_2=CHCH_2X > EtX >$
$> Me_2CHX > Me_3CX > > Me_3CCH_2X > CH_2=CHX > > PhX > HC(CH_2CH_2)_3CX$
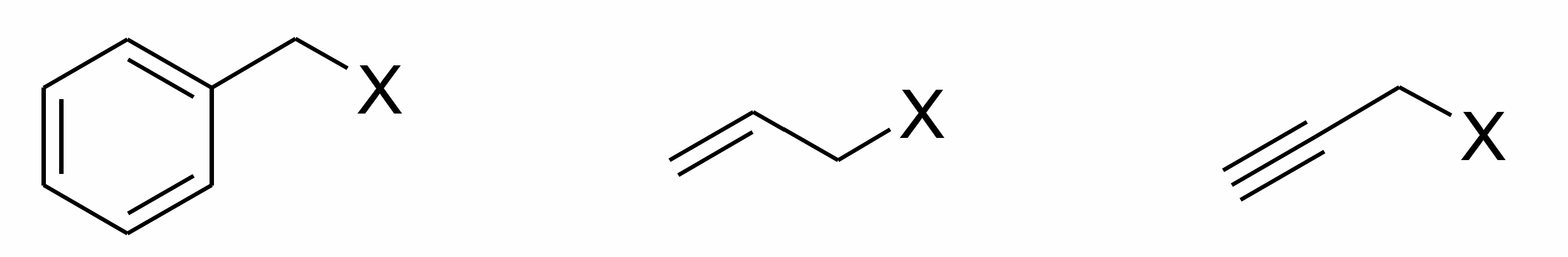
Наиболее реакционноспособны в $S_N2$ реакциях бензильные, аллильные и пропанильные субстраты:
-
Нуклеофильности реагента и его концентрации. Чем больше нуклеофильность реагента, тем больше вероятность прохождения реакции по $S_N2$-механизму. Кроме этого, высокие концентрации способствуют $S_N2$-реакции, а низкие – $S_N1$.
-
Природа растворителя влияет на сольватацию исходных соединений и ионов, образующихся при диссоциации галогенпроизводных углеводородов. Оптимальные растворители для $S_N2$ реакций - апротонные полярные (DMF, DMSO; $CH_3CN$, ацетон).
Замечание 4В случае реакций с $S_N2$-механизмом менее полярное переходное состояние сольватируется меньше, чем исходные соединения. Поэтому с увеличением полярности растворителя скорость таких реакций уменьшается.
-
Природа галогена, который замещается, влияет на скорость реакции закономерно уменьшению поляризуемости связи $C-Hal$ в ряду: $R-I > R-Br > R-Cl >> R-F$.