Стереоизомеры, их виды
Стереоизомеры – это вещества, в молекулах которых атомы связаны между собой одинаково, но расположение их в пространстве различно.
Стереоизомеры подразделяют на:
- Энантиомеры (оптические изомеры). Имеют одинаковые физико – химические свойства (плотность, температуру кипения и плавления, растворимость, спектральные свойства) в ахиральном окружении, но различную оптическую активность.
- Диастеромеры – это соединения, которые могут содержать два и более хиральных центра.
Под хиральностью понимают способность объекта не соответствовать своему зеркальному отражению. То есть, молекулы, не обладающие зеркально – поворотной симметрией, являются хиральными.
Прохиральная молекула – это молекула, которая может быть превращена в хиральную единственным изменением любого ее фрагмента.
В хиральных и прохиральных молекулах некоторые группы ядер, на первый взгляд химически эквивалентные, являются магнитно неэквивалентными, что подтверждают спектры ядерного магнитного резонанса. Это явление называется диастереотопией ядер, может наблюдаться по спектрам ядерного магнитного резонанса при наличии в одной молекуле прохирального и хирального фрагментов.
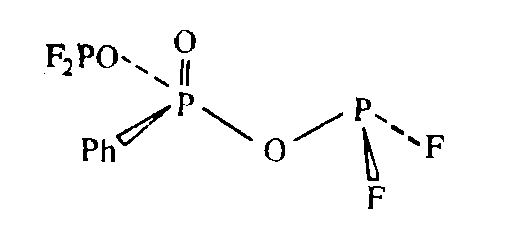
Например, в прохиральной молекуле две группы OPF2 являются эквивалентными, но в каждой группе атомов $PF_2$ атомы фтора неэквивалентны.
Это проявляется в константе спин – спинового взаимодействия 2/$FF$.
Если молекула оптически активная, то неэквивалентность ядер Х в тетраэдрических группах –$MX_2Y$ (например, -$CH_2R$, -$SiH_2R$ и др.) или пирамидальных группах –$MX_2$ (например, -$PF_2$, -$NH_2$ и др.) не зависит от высоты барьера внутреннего вращения этих групп. При вращении плоских групп –$MX_2$ и тетраэдрических –$MX_3$ потенциальный барьер очень низок, в результате чего ядра $X$ становятся эквивалентными.
Построение названий хиральных молекул
Современная система построения названий для хиральных молекул предложена Ингольдом, Каном и Прелогом. Согласно этой системе, для всех возможных групп $A$, $B$, $C$, $D$ при асимметричном атоме углерода выясняется порядок старшинства. Чем больше атомный номер, тем он старше:
$H$
Если атомы одинаковые, то сравнивают второе окружение:
$CH_3$
Предположим, что группы расположены по уменьшению старшинства: $A → B → C → D$. Развернем молекулу таким образом, чтобы младший заместитель $D$ был направлен за плоскость рисунка, от нас. Тогда понижение старшинства в остальных группах может происходить либо по часовой, либо против часовой стрелки.
Если понижение старшинства происходит по часовой стрелке при обозначении изомера используют символ $R$ (правый), если против часовой стрелки – $S$ (левый). Понятия «левый» и «правый» не отражают реального направления вращения линейно поляризованного света.
Эмиль Фишер предложил $DL$ –номенклатуру, согласно которой правовращающийся энантиомер обозначается буквой $D$, а левовращающийся – $L$. Эта номенклатура широко используется для обозначения аминокислот и углеводов.
Стереоспецифичность физиологической активности оптических изомеров
Оптические изомеры проявляют разную физиологическую активность. Активные центры ферментов и рецепторы состоят из аминокислотных остатков, которые являются оптически активными элементами.
Рецептор распознает физиологически активную молекулу по принципу «ключ в замке». При присоединении молекулы субстрата, активный центр меняет свою геометрию.
Например, никотиновый алкалоид содержит один центр оптической изомерии и может существовать в виде двух энантиомеров. $S$ - изомер расположен справа и является ядом для человека (летальная доза 20 мг), $R$- изомер менее ядовит:
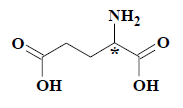
$L$ – глутаминовую кислоту
широко используют в качестве усилителя вкуса мяса при приготовлении консервов. $D$ - глутаминовая кислота такими свойствами не обладает.
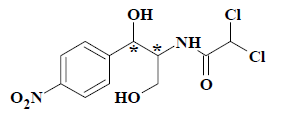
В соединении
есть два асимметричных атома углерода, следовательно, возможно существование 4 изомеров ($2^n$). Но только один ($R,R$)-изомер – хлоромицетин - проявляет свойства антибиотика
Получение чистых оптических изомеров является важной химико – технологической проблемой.
Пути получения чистых энантиомеров:
- Выделение из природного сырья. Все природные углеводы относятся к $D$-ряду, а природные аминокислоты – к $L$-ряду. Возможно использовать эти изомеры в химических реакциях, не затрагивающих центры оптической изомерии. Таким способом можно получить узкий круг веществ.
-
Выделение необходимого изомера из рацемической смеси при помощи оптически активного реагента.
Пример 1Необходимо разделить смесь изомеров 1-фенилэтиламина. Вначале получают соли фенилэтиламина с природной винной кислотой (с ($R,R$)-изомером). Соли ($R,R,R$) и ($S,R,R$) являются диастереомерами и обладают разными физико – химическими свойствами. Их разделяют перекристаллизацией из этилового спирта.
-
Асимметрический синтез. Этот путь является самым перспективным. Необходимо, чтобы молекула имела один хиральный центр. Если во время реакции возникает второй центр, то переходные состояния будут диастереомерами, обладающими разной энергией. Если разность их энергий достигнет 10 кДж/моль, то доля определенного изомера (стереоселективность) достигнет 98%.