Как уже указывалось раннее, промежуточные интермедиаты - пентадиенильные катионы подвергаются только одной реакции - потере протона (или дейтрона в случае с изотопными маркерами). В этой рееакции, восстанавливается ароматическая $\pi$-система, и она является более быстрой, чем реакция с водой. В алкилых катионах взаимодействие с нуклеофильными частицами намного важнее реакцией, потому что отщепление протона от таких карбокатионов не имеет такой дополнительной "движущей силы", как образование ароматического кольца.
Кинетические изотопные эффекты реакций, идущих с отщеплением протона
Роль отщепления протона от комплексов промежуточных интермедиатов в реакциях электрофильного ароматического замещения может быть показана при изучении первичных кинетических изотопных эффектов (КИЭ) водорода. Для реакций, идущих по механизму электрофильного замещения, изотопные эффекты отсутствуют. Например, изотопные эффекты не наблюдаются в реакциях нитрования, хлорирования, бромирования и алкилирования по Фриделю-Крафтсу. Реакции ацилирования аренов характеризуются чрезвычайно низкими КИЭ. С другой стороны, изотопные эффекты имеют заметную величину в реакциях сульфирования, азосочетания и других реакциях.
Причины возникновения первичных кинетических изотопных эффектов заключаются в различных внешних и внутренних факторах.
Варианты зависимости хода процессов от стадии отщепления протона
Исходя из сопоставления КИЭ и экспериментальных данных, возможны три варианта зависимости хода процессов от стадии отщепления протона:
- В ряде процессов КИЭ имеют предсказываемые теорией значения. Если величины изотопных эффектов лежат в указанных интервалах, то вывод о механизме реакции однозначен: скорости реакций определяются переносами протонов с образованием линейных переходных состояний, в которых атомы водорода расположены симметрично между донорами и акцепторами электронов.
- Существует и другой крайний случай, в котором обычно указывается на то, что стадии переноса водорода не определяют скорости реакций.
- Средние значения КИЭ могут указывать на то, что общие скорости реакций частично определяются скоростями переноса протонов. В этих случаях величину изотопного эффекта можно изменить путем изменения концентрации реагента, к которому переходит протон в данной реакции. В электрофильном ароматическом замещении наблюдается как раз такая ситуация. Но средние по величине изотопные эффекты интерпретировать крайне трудно.
В общем виде механизм электрофильного ароматического замещения можно записать следующим образом (без учета $\pi$-комплексов):
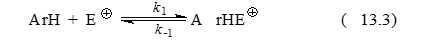
Рисунок 1.
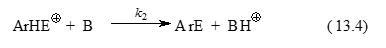
Рисунок 2.
Общие закономерности механизма электрофильного ароматического замещения
Резюмируя вышесказанное, можно сделать вывод, что большинство реакций электрофильного ароматического замещения имеют общий механизм присоединения–отщепления с образованием в качестве нестабильных короткоживущих интермедиатов аренониевые ионы - $\sigma$-комплексы. На начальной стадии реакций аренов с электрофилами образуются $\pi$-комплексы - слабые, как правило быстрораспадающиеся, соединения. Однако таких бесспорных случаев, в которых было бы точно доказано, что самой медленной стадией таких реакций буде образование именно $\pi$-комплексов.
На стадиях отщепления протонов от $\sigma$ -комплексов во многих случаях процесс происходит крайне быстр. Однако в при некоторых условиях, например при недостатке основания, этот процесс замедляется. В этих случаях наблюдаются кинетические изотопные эффекты водорода. В определенных придельных условиях, которые достаточно редки в реальных процессах, стадии отщепления протонов могут стать определяющими скорости процесса.











