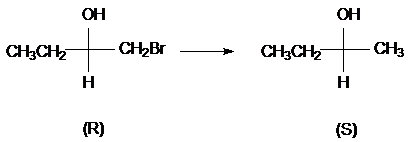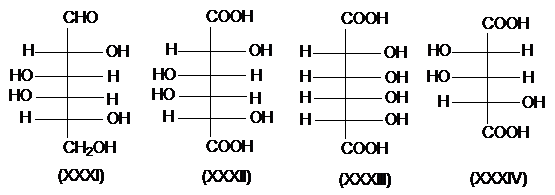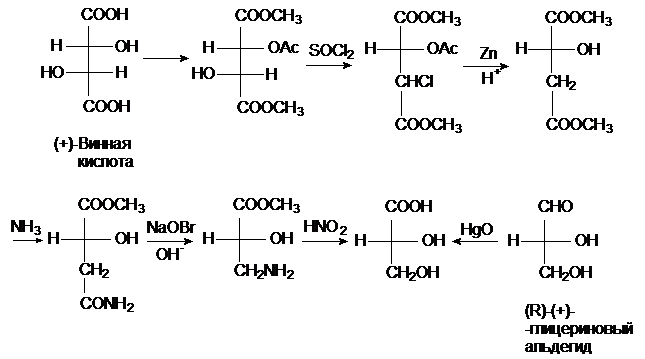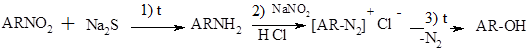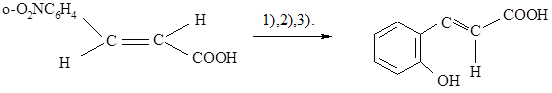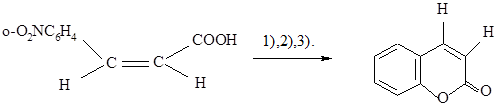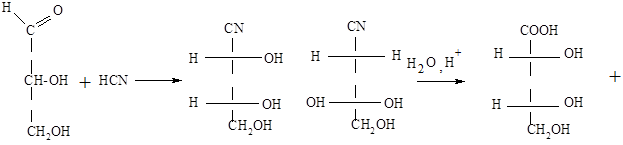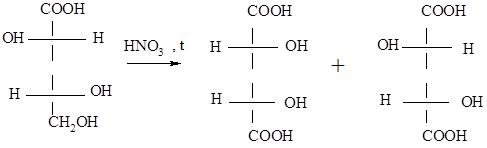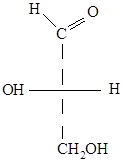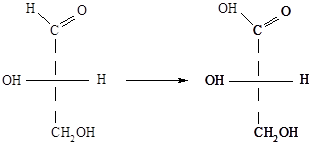Химические методы определения относительной конфигурации изомера, очень разнообразны.
К первой группе химических методов относятся превращения соединений с неизвестной конфигурацией в соединения с известной конфигурацией или образование искомой конфигурации из без нарушения хиральных элементов, например, хиральных центров. Поскольку в ходе превращений хиральные центры не затрагиваются, очевидно, что продукты должны иметь ту же конфигурацию, что и исходные соединение.
При этом вовсе не обязательно, соблюдение того что если неизвестные соединения относятся к ($R$)-ряду, то и известные будет иметь ($R$)-конфигурации. Например, восстанавливая ($R$)- 1-бром-2-бутанол в 2-бутанол, при котором не затрагивается хиральный центр, продуктом можно получить изомер ($S$)- конфигурации несмотря на то, что конфигурация соединения не изменилась. Это связано с тем, что группа $CH_3CH_{2^-}$ младше группы $BrCH_{2^-}$, но старше группы -$CH_3.$
Рисунок 1.
Установление относительных конфигураций углеводов
Примером химической корреляции является установление относительных конфигураций углеводов путем их окисления. В частности так можно определить конфигурацию $D$-галактозы (XXXI). Поскольку процесс окисления приводит к образованию оптически неактивных дикарбоновых кислот, относительные конфигурации их четырех оптических центров могут соответствовать или структуре XXXII, или структуре XXXIII. Но дикарбоновая кислота (XXXIV), полученная из галактозы путем отщепления альдегидного атома углерода, будет оптически активной. Следовательно, $D$-галактоза будет иметь относительную конфигурациию, показанную формулой XXXI:
Рисунок 2.
Аналогичное превращение с $L$-галактозой дает такой же результат, за исключением противоположного знака для оптического вращения.
Но следует заметить, что этим путем можно установить лишь относительные конфигурации исследуемых молекул (в данном случае XXXI и XXXII), но не их абсолютные конфигурации.
Ниже приведен пример схемы конфигурационных корреляций (+)-винной кислоты с (+)-($R$)-глицериновым альдегидом на основе превращений, которые не затрагивают асимметрический центр.
Рисунок 3.
Определение конфигурации π-диастереомеров химической корреляцией
Другим примером явлется определение конфигурации нитрокоричных кислот (серией химических превращений (восстановление, диазотирования, замена диазо группы на группу $OH$) через о аминокорични и о диазокорични кислоты получают о гидроксикоричные кислоты:
Рисунок 4.
Установив, какой из стереоизомеров $о$-нитрокоричной кислоты дает кумаровую, а какой непрямую кислоту (фактически не кислоту, а ее лактон – кумарин), можно тем самым доказать, которая из о-нитрокоричних кислот имеет транс-, а какая цис- конфигурацию:
Рисунок 5. Транс- конфигурация. Автор24 — интернет-биржа студенческих работ
Рисунок 6. Цис- конфигурация. Автор24 — интернет-биржа студенческих работ
Определение конфигурации σ-диастереомеров и энантиомеров химической корреляцией
При подходе к проблеме конфигурации энантиомеров возникают некоторые трудности. Мы знаем, что один антипод поворачивает вправо, другой влево. Но на самом деле знак поворота - это чисто внешний признак, не более чем температура плавления или окраска вещества. Он не связан прямо с пространственной конфигурацией; более того, известны примеры, когда знак вращения меняется в зависимости от условий - растворителя, температуры, даже концентрации.
Итак имеем два вещества, одно из которых мы узнаем по (+) -, другую по (-) - вращению; известно, что им соответствуют две зеркальные формулы. Надо определить, какая формула которому антиподу отвечает.
На сегодняшний день существует рентгенографический метод определения абсолютной конфигурации, уже рассмотренный ранее.
Этим методом доказано, что (+) - винная кислота имеет конфигурацию:
Абсолютные конфигурации, определены рентгенографическим методом, и лежат в основе стереохимических корреляций.
В качестве примера можно привести корреляции конфигурации глицеринового альдегида и винной кислоты. Взяв в качестве исходного реагента левовращающий изомер глицеринового альдегида и считая, что абсолютная конфигурация для него пока не известна, к нему применяют цепь реакций удлинения углеродного скелет вещества. Последовательно проводят присоединение $HCN$, гидролиз и наконец, окисление первичной спиртовой группы. Проведенные реакции не затрагивают центр хиральности:
Рисунок 7.
При этом образуются две стереоизомерных винные кислоты, поскольку новый асимметричный центр тоже возник в двух конфигурациях:
Рисунок 8.
В мезовинной кислоте конфигурации асимметричных центров противоположны и какой из них был в исходном глицериновом альдегиде, установить невозможно. Поэтому мезовинная кислота не используется для установления конфигурации. Второй продукт реакции - право обращающая винная кислота с двумя одинаковыми асимметричными центрами. Учитывая, что один из них находится в исходном (-) - глицериновом альдегиде и зная абсолютную конфигурацию (+)- винной кислоты, ясно, что (-)- глицериновый альдегид имеет конфигурацию:
Рисунок 9.
Далее, с исходным (-)- глицериновым альдегидом проводят ряд химических превращений и получают винную кислоту. После этого выполняют поляриметрические измерения, чтобы выяснить, какая из антиподных винных кислот образовалась. Узнав, что получили (+)- винную кислоту, абсолютная конфигурация которой установлена по рентгеноструктурным данным, делают вывод, что такая же была и конфигурация исходного (-)- глицеринового альдегида.
Теперь когда известна конфигурация (-) - глицеринового альдегида методом преобразований можно получить вещество о строении которой можно говорить, например (+) - глицериновую кислоту:
Рисунок 10.