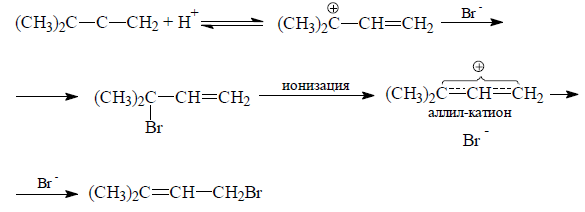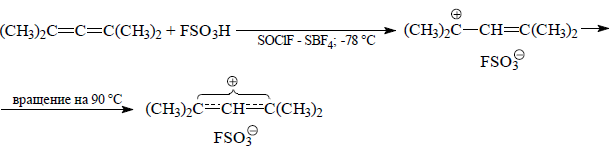Присоединение галогеноводородов
Электрофильная частица (протон) может присоединяться к центральному или концевому атому углерода аллена:
При присоединеии протона к центральному атому образуется аллильный катион

Рисунок 1.
У полученного катиона пустая $p$-орбиталь перпендикулярна электронам π-связи, поэтому по формальным признакам его можно отнести к аллильным карбокатионам.
При присоединении протона в качестве промежуточного вещества образуется винильный карбокатион. Положительный заряд локализован на центральном атоме углероде, $p$-электроны перпендикулярны $p$-орбитали, которая несет положительный заряд, поэтому оставшаяся π-связь не принимает участия в стабилизации карбокатиона.

Рисунок 2.
Первичный аллильный карбокатион является менее стабильным, чем вторичный винильный карбокатион. Присоединение галогеноводородов $HBr$, $HCl$, $HI$ к аллену происходит региоспецифично, с образованием таких продуктов реакции, у которых галоген находится у центрального атома углерода:

Рисунок 3.
Следовательно, при присоединении галогеноводорода к аллену, дейтерий в продуктах реакции будет расположен только в метильной группе:

Рисунок 4.
Это согласуется с механизмом образования винильного катиона в роли интермедиата.
Например: Взаимодействие с $HCl$ 1,2-бутадиена и 2,3-пентадиена во много раз проходит быстрее, чем с пропадиеном, что указывает на электрофильный характер присоединения галогеноводородов к алленам.
Если в аллене присутствуют две алкильные или одна арильная группы, то региоселективность присоединения $HHal$ полностью изменяется:

Рисунок 5.
Протон атакует центральный sp-гибридизованный атом углерода, в результате чего образуется аллильный карбокатион.
Последующие превращения протекают по схеме:
Рисунок 6.
При протонировании аллена по центральному атому углерода появляется аллил – катион. В нем π-электроны двойной связи ортогональны пустой р-орбитали и не принимают участия в делокализации положительного заряда.
Ион галогена присоединяется по пустой $p$-орбитали, в результате чего образуется третичный аллильный галогенид, который далее ионизируется по $SN1$-механизму. Возникает плоский аллил – катион, способный присоединить галогенид-ион к наименее замещенному концевому атому карбона.
Реакция протекает благодаря тому, что термодинамическая стабильность первичного аллилгалогенида выше термической стабильности третичного аллилгалогенида.
Например: Исключительно по центральному $sp$-гибридному атому углерода будет присоединяться протон в соединениях: 1,3-диметилаллен, 1,1-диметилаллен, 1,1,3,3-тетраметилаллен (реакция протекает в суперкислой среде $FSO_3H-SbF_5$ при -78ºС).
Рисунок 7.
Присоединение галогенов
Присоединение пропандиеном молекул галогена проходит в два этапа. Первая молекула галогена ($Cl$, $Br$) присоединяется легко в мягких условиях. Образуется 2,3-дигалогенпропен. Вторая молекула галогена присоединяется уже намного медленнее и приводит к появлению 1,2,2,3-тетрагалогенпропана:

Рисунок 8.
Для реакций присоединения галогенов справедлив механизм, содержащий появление аллильного или винильного карбокатиона и последующее присоединение галогенид-иона. Для аллена наиболее вероятным является образование винильного карбкатиона:

Рисунок 9.
В 1-алкил-, 1,1-диалкил- и 1,3-диалкилалленах электрофильному воздействию подвергается центральный $sp$-гибридный атом углерода, а галогенид-ион присоединяется к концевому атому углерода карбокатиона.
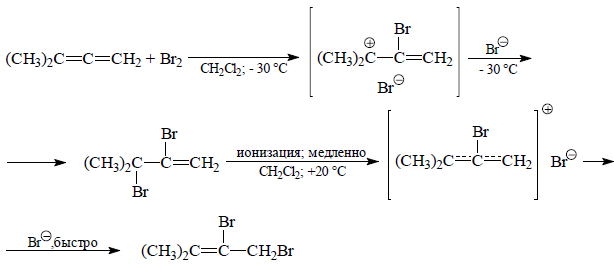
Например: Присоединение брома к 3-метилбутадиену-1,2 при -30ºС. В результате образуется дибромид – третичный аллильный бромид.
Рисунок 10.
При нагревании до +20ºС дибромид полностью изомеризуется в 1,2-дибром-3-метилбутен-2.
Присоединение сульфенгалогенидов
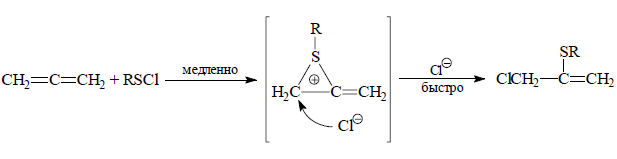
Присоединение к аленнам сульфенгалогенидов $RS^{σ^+}-Hal^{σ^-}$ происходит таким образом, что группа $RS^{σ^+}$ всегда присоединяется к центральному $sp$-гибридному атому углерода, а галоген к атому $C$(1) или $C$(3) диена:
Рисунок 11.
Цикл расщепляется в результате $SN2$-атаки галогенид-иона по концевому атому углерода. Присоединение $RSCl$ к аллену имеет схожий механизм с присоединением сульфенхлорида и галогена к диенам.
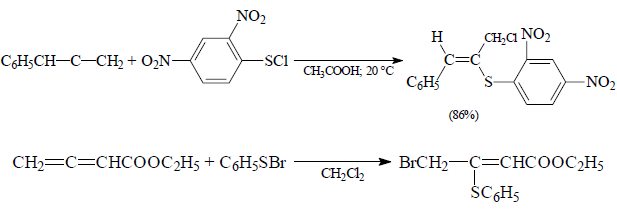
В случае ннесимметричных алленов, сульфенхлориды присоединяются по наиболее замещенной двойной связи:

Рисунок 12.
Гидроксимеркурирование
Взаимодействие 1,2-аллена с ацетатом ртути по своей региоселективности подобен реакции гидрогалогенирования диенов.
Электрофил $(Hg(OAc))^+$ взаимодействует с концевым атомом аллена с образованием продукта сопряженного присоединения метилат-иона из метилового спирта:
Рисунок 13.
Однако взаимодействие алленов вида $R_2C=C=CH$ (3-метилбутадиена-1,2) с $(Hg(OAc))^+$ осуществляется по центральному углеродному атому.