Что такое изотермический процесс
Изотермическим процессом называется процесс, происходящий в неизменной массе газа при постоянной температуре.
Запишем уравнение для двух состояний идеального газа:
\[p_1V_1=\nu RT\left(1\right),\] \[p_2V_2=\nu RT\ \left(2\right).\]Закон Бойля-Мариотта
Разделим уравнение (2) на уравнение (1), получим уравнение изотермического процесса:
\[\frac{p_2V_2}{p_1V_1}=1\ (3)\]или
\[pV=const\ \left(4\right).\]Уравнение (4) называют законом Бойля-Мариотта.
Этот процесс происходит с подводом тепла, если объем увеличивается, или его отводом, чтобы уменьшать объем. Запишем первое начало термодинамики, последовательно получим выражения для работы, внутренней энергии и количества теплоты изотермического процесса:
\[\delta Q=dU+dA=\frac{i}{2}\nu RdT+pdV,\ \left(5\right).\]Температура не изменяется, следовательно, изменение внутренней энергии равно нулю ($dU=0$). Получается, что в изотермическом процессе все подводимое тепло идет на совершение газом работы:
\[\triangle Q=\int\limits^{V_2}_{V_1}{dA}\left(6\right),\]где $\delta Q\ $- элементарное тепло, подводимое к системе, $dA$- элементарная работа, которую совершает газ в процессе, i - число степеней свободы молекулы газа, R -- универсальная газовая постоянная, d -количество молей газа, $V_1$- начальный объем газа, $V_2$- конечный объем газа.
\[A=\int\limits^{V_2}_{V_1}{pdV}\left(7\right).\]Используем уравнение состояния идеального газа, выразим из него давление:
\[pV=\nu RT\to p=\frac{\nu RT}{V}\left(8\right).\]Подставим уравнение (8) в подынтегральное выражение уравнения (7):
\[A=\int\limits^{V_2}_{V_1}{\frac{\nu RT}{V}dV}=\nu RT\int\limits^{V_2}_{V_1}{\frac{dV}{V}}=\nu RTln\left(\frac{V_2}{V_1}\right)\left(9\right).\]Уравнение (9) -- выражение для работы газа в изотермическом процессе. Уравнение (9) можно записать через отношение давлений, если использовать закон Бойля-Мариотта, в таком случае:
\[A=\nu RTln\left(\frac{p_1}{p_2}\right)\left(10\right)\] \[\triangle Q=A\ (11),\]Уравнение (11) определяет количество теплоты, сообщаемое газу массы m в изотермическом процессе$.
Изопроцессы очень часто изображают на термодинамических диаграммах. Так, линия, изображающая на такой диаграмме изотермический процесс, называется изотермой (рис.1).
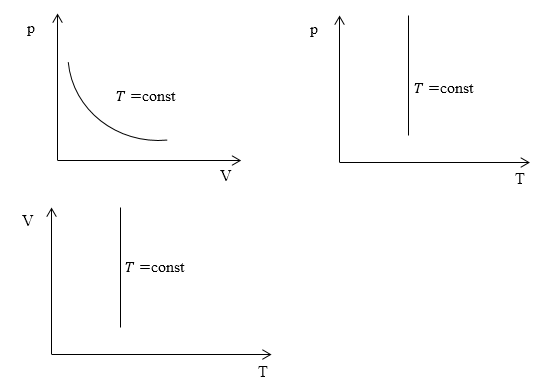
Рис. 1
Задание: Идеальный одноатомный газ расширяется при постоянной температуре от объема $V_1=0,2\ м^3$ до $V_2=0,6\ м^3$. Давление в состоянии 2 равно $p_2=1\cdot {10}^5\ Па$. Определить:
- Изменение внутренней энергии газа.
- Работу, которую совершает газ в этом процессе.
- Количество теплоты, получаемое газом.
Решение:
Так как процесс изотермический, то внутренняя энергия газа не изменяется:
\[\triangle U=0.\]Из первого начала термодинамики, следовательно:
\[\triangle Q=A\ \left(1.1\right).\] \[A=\nu RTln\left(\frac{V_2}{V_1}\right)\left(1.2\right).\]Запишем уравнение конечного состояния идеального газа:
\[p_2V_2=\nu RT\to T=\frac{p_2V_2}{\nu R}\ \left(1.3\right).\]Подставим выражение для температуры из (1.3) в (1.2), получим:
\[A=\nu R\frac{p_2V_2}{\nu R}ln\left(\frac{V_2}{V_1}\right)=p_2V_2ln\left(\frac{V_2}{V_1}\right)\left(1.4\right).\]Так как все величины в данных находятся в СИ, проведем расчет:
\[A=0,6\cdot {10}^5ln\left(\frac{0,6}{0,2}\right)=0,6\cdot {10}^5\cdot 1,1=6,6{\cdot 10}^4(Дж)\]Ответ: Изменение внутренней энергии газа в заданном процессе равно нулю. Работа, которую совершает газ в этом процессе $6,6{\cdot 10}^4Дж.$ Количество теплоты, получаемое газом в данном процессе, $6,6{\cdot 10}^4Дж$.
Задание: На рис 2. представлен график изменения состояния идеального газа массы m в осях p(V). Перенесите этот процесс в оси p(T).
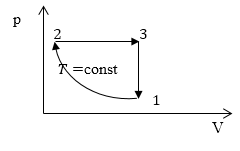
Рис. 2
Решение:
Опишем данный на рисунке 2 круговой процесс.
1-2 изотермический процесс ($T=$const), в котором объем уменьшается (V$\downarrow $), давление растет (p$\uparrow $).
2-3 изобарический процесс ($p=$const), в котором V$\uparrow $, следовательно, из закона Гей-Люссака, T$\uparrow .$
3-1 изохорный процесс (V$=const$), в нем p$\downarrow $, следовательно, из закона Шарля T$\downarrow $.
Изобразим в осях p(T) вышеперечисленные процессы.
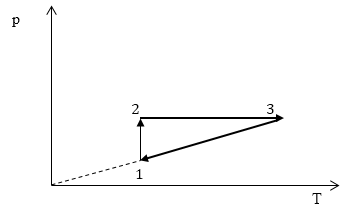
Рис. 3
Задание: Какой график на рис. 4 представляет изотермический процесс?
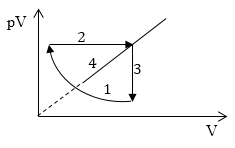
Рис. 4
Решение:
Изотермический процесс описывается законом Бойля-Мариотта
\[pV=const\ \left(3.1\right).\]Следовательно, на графике в осях $pV(V)$ изотерма представлена графиком 2.
Ответ: График 2.











